Комплекс I обеспечивает окисление молекулы NADH, а комплекс II окисляет молекулу FADH 2, электроны поступают на коферменты электрон-транспортной цепи и в конце концов поступают на молекулу убихинона или кофермента Q. Кофермент Q – хиноновое производное с длинным изопреноидным хвостом. Его называют также убихиноном из-за его повсеместного распространения в биологических системах.
Число изопреновых единиц в коферменте Q зависит от вида живых организмов, У млекопитающих его наиболее распространенная форма содержит десять изопреновых единиц и обозначается как Q 10. Изопреноидный хвост обуславливает высокую неполярность Q, которая способствует его быстрой диффузии в углеводородной фазе внутренней митохондриальной мембраны. Кофермент Q является компонентом митохондриальных липидов; среди других липидов преобладают фосфолипиды, являющиеся частью митохондриальной мембраны. Структура кофермента Q сходна со структурой витаминов К и Е.
Близкую структуру имеет и пластохинон, находящийся в хлоропластах. Все эти вещества имеют в своей структуре полиизопреноидную боковую цепь. Содержание кофермента Q значительно превосходит содержание других компонентов дыхательной цепи (по параметру стехиометрии); это позволяет предположить, что кофермент Q является подвижным компонентом дыхательной цепи, который получает восстановительные эквиваленты от фиксированных флавопротеиновых комплексов и передает их на цитохромы. Кофермент Q-единственный переносчик электронов в дыхательной цепи, который не связан прочно с белком и не присоединен к нему ковалентно. Кофермент Q действительно служит высокомобильным переносчиком электронов между флавопротеинами и цитохромами цепи переноса электронов.
Убихинон-цитохром с редуктаза (комплекс III) включает 11 субъединиц с молекулярным весом: 49,5, 47, 44, 28, 21,5, 13,5, 9,5, 9, 8, 7, 6,5 kDa соответственно. Третья субъединица весом 44 kDa присоединяет две молекулы гемов b H и b L . Центральную роль цитохромов в дыхании открыл в 1925 г. Дэвид Кейлин (David Keilin).
Цитохром – это переносящий электроны белок, молекула которого содержит в качестве простетической группы гем.
Гем – это модифицированная молекула тетрапиррольного кольца, в центре которой ассоцииирован ион металла (это могут быть ионы железа, меди и других металлов). В зависимости от радикалов, модифицирующих кольцо, и от ионов ассоцированных с кольцом гема, выделяют несколько классов цитохромов. Субъединица V или белок Риске содержит Fe 2-S 2кластер. Субъединица VI связывает убихинон, субъединица IV координирует цитохром с. Функции остальных субъединиц не выявлены или участвуют в организации комплекса (схема функционирования убихинона и коферментов комплекса III представлена на рисунке 13).
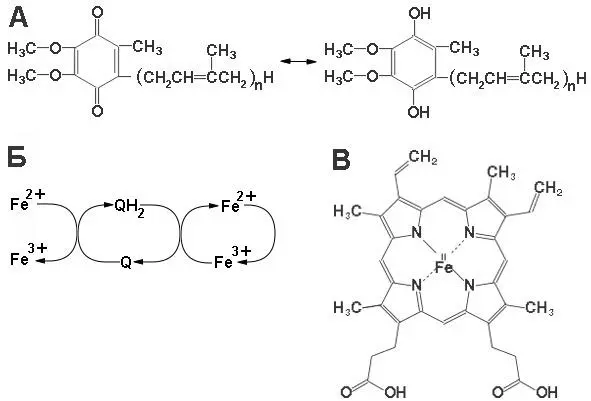
Рисунок 13: А – схема окислительно-восстановительной реакции с убихиноном; Б – схема окислетельно-восстановительных реакций между FeS белком и убихиноном, между убихиноном и гемом; В – структура гема в цитохромах
Электроны с убихинон-цитохром с редуктазы переносятся на цитохром с. Цитохром с – водорастворимый, подвижный белок с молекулярной массой 12 kDa. Этот белок мигрирует между комплексами III и IV в межмембранном пространстве.
Цитохром оксидаза (комплекс IV) содержит восемь белковых субъединиц, с ними ассоциированы два гема, содержащих ионы меди, которые называют гемы а и а3. Кроме этого содержит два иона меди Cu Aи Сu B. Центр Сu Bпредставляет ион меди соединенный с радикалами трех остатков гистидина. Центр Cu Aсодержит два атома меди расположенных очень близко и скоординированных с белком (схема функционирования коферментов комплекса IV представлена на рисунке 14).
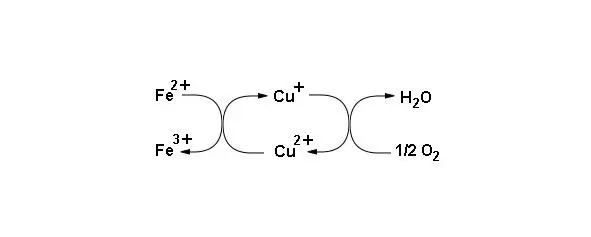
Рисунок 14: Схема функционирования коферментов комплекса IV
Механизмы переноса электронов в электронтранспортной цепи
Первый комплекс или NADH-дегидрогеназа взаимодействует с молекулой NADH, электроны переносятся на (FMN), в результате FMN принимает с NADH два электрона и два протона от среды, и образуется NAD+ и FMNH 2, затем электроны переносятся на первый комплекс Fe 4-S 4белка в результате происходит окисление FMNH 2и перенос электронов на ион железа Fe-S белка, далее железо в комплексе восстанавливается из положения Fe 3+до Fe 2+. Это происходит потому, что окислительно-восстановительный потенциал NADH меньше, чем у FMN, поэтому происходит окисление NADH флавинмононуклеотидом, который затем окисляется Fe 4-S 4 белком, чей окислительно-восстановительный потенциал еще больше. Далее происходит серия окислительно-восстановительных реакций с участием Fe-S белков, каждый из которых является большим окислителем, чем предыдущий.
Читать дальше
Конец ознакомительного отрывка
Купить книгу














