Я не стану вдаваться в детали работы этих двух джентльменов – она в достаточной мере описана в других источниках, в частности на сайте Фонда Нобеля, так как оба они стали лауреатами Нобелевской премии за исследования L-допы: Карлссон получил премию в 2000 году за достижения в области физиологии или медицины, а Ноулз в 2001 году был награжден премией по химии. Однако важнейшей частью промышленного способа производства L-допы является катализ с использованием ценного металла родия, а поскольку катализ – центральная концепция современной химии, этот процесс заслуживает дальнейшего рассмотрения.
К настоящему моменту у вас есть хотя бы туманное представление о катализаторах – веществах, которые заставляют химическую реакцию идти гораздо быстрее, не расходуясь при этом в процессе; однако вы, возможно, не осознаете фундаментальной важности, которую это понятие будет иметь для нас в будущем. Если химическая реакция протекает недостаточно быстро, то что нам делать в отсутствие подходящего катализатора? Мы задаем ей взбучку, чаще всего при помощи тепла, и если делать это круглосуточно, то затраты на энергию будут очень высоки. Другая проблема – то, что мы называем выходом реакции и побочными продуктами. Хороший катализатор превращает большее количество реагентов в полезный продукт и производит меньше отходов. Не менее важно и то, что в этом случае будет меньше проблем с отделением полезных веществ от нежелательных молекул, так как в большинстве промышленных химических процессов эта задача требует существенных энергозатрат.
Ноулз и его сотрудники создали родийсодержащую молекулу, в которой одну сторону маленького иона металла прикрывает органическая молекула, использующая для связи с родием фосфор [292] Knowles W.S. Nobel Lecture // Les Prix Nobel: The Nobel Prizes 2001. Nobel Foundation, 2002.
. Эта органическая молекула уже обладает вышеупомянутой хиральностью, и, несмотря на то что реакция протекает на атоме родия, эта хиральность определяет, какая из двух возможных молекул допы образуется. После реакции с участием газообразного водорода и исходного вещества от атома родия отделяется одна молекула L-допы, что позволяет всей структуре из родия и прикрепленной к нему фосфорной органической молекулы вернуться в исходное состояние, а весь процесс может начинаться заново.
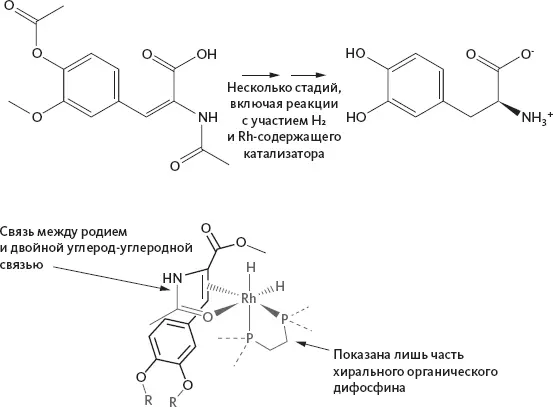
Рисунок 49. Вверху : Упрощенная реакционная схема, показывающая превращение ахирального исходного реагента в энантиомерно (оптически) чистый продукт. Эта реакция протекает в несколько стадий, но хиральность создается родиевым катализатором. Внизу : схематическое изображение родиевого катализатора в действии. Жирными линиями показаны те атомы, которые станут молекулой L-допы [293] Elschenbroich C., Salzer A. Organometallics: A Concise Introduction. VCH, Weinheim, 1989.
.
У катализатора есть лишь одно важное ограничение: это не философский камень, и поэтому катализ не может нарушать законы термодинамики. Невозможно найти катализатор, который превратит воду и углекислый газ в топливо, потому что, выражаясь языком термодинамики, это реакция с возрастающей энергией. Те реакции, которые мы можем осуществлять на практике, – убывающие с точки зрения свободной энергии Гиббса (с которой мы встречались, когда обсуждали наполеоновские пуговицы), что, заметим, отличается от утверждения о том, что во всех самопроизвольных реакциях выделяется тепло.
Термодинамика, особенно химическая, – весьма увлекательный предмет, но многие студенты считают ее трудной. Мне кажется, отчасти проблема заключается в том, что сначала термодинамика утверждает очевидное, но при этом с большим количеством математических подробностей, и это вгоняет всех в сон; а когда студенты просыпаются, лектор уже добрался до частных производных и символов S, G и μ, и студентам очень трудно наверстать упущенное. Это как если бы кому-то объясняли правила крикета и человек заснул на словах о том, что отбивающий бьет по мячу, а проснулся уже в разгаре игры.
Для меня термодинамика – это здравый смысл сквозь призму математики. Вы вдруг видите вещи гораздо более отчетливо, изучаете прежде скрытые взаимосвязи и приходите к выводам, которых раньше не замечали. Например, начав с известного количества молекул А и В – скажем, углекислого газа и воды, – вы можете подсчитать, сколько C и D – например, октана (углеводородной молекулы в составе бензина) и кислорода – вы можете получить при любой заданной температуре: оказывается, нисколько, потому что энергия Гиббса возрастает в этой реакции при любых условиях. Не повезло: таким простым путем решить проблему глобального потепления не выйдет.
Читать дальше
Конец ознакомительного отрывка
Купить книгу













