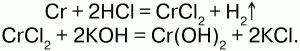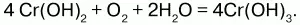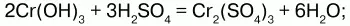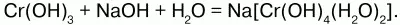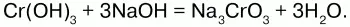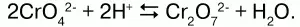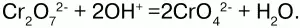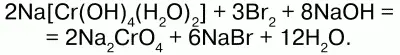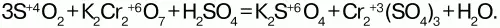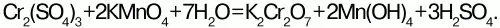Гидроксид хрома II Сг(ОН)2желтого цвета, в воде не растворим, обладает основными свойствами, является восстановителем, получается действием щелочи на хлорид хрома CrСl2, получаемого при взаимодействии Cr c НСl:
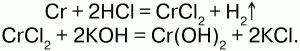
Соединения Cr II неустойчивы и легко окисляются кислородом воздуха:
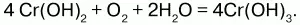
Гидроксид хрома III (Cr(OH)3)n– это сложный полимер зеленого цвета, не растворимый в воде, обладает амфотерными свойствами – растворяется в кислотах и в щелочах; реагирует с кислотами с образованием солей хрома (III):
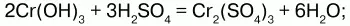
со щелочами – с образованием сине-фиолетовых растворов – гидроксохромитов:
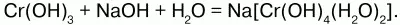
При сплавлении Cr(ОН)3 со щелочами получают хромиты, а с избытком – метахромиты:
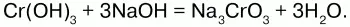
Хроматы– соли хромовой кислоты Н2Сг04,существующей лишь водных растворах с концентрацией не выше 75 %. Валентность хрома в хроматах – 6. Хроматы щелочных металлов и магния имеют хорошую растворимость в воде, а растворимость щелочноземельных металлов очень резко снижается в ряду CaCrO4 – SrCrO4 – BaCrO4 – RaCrO4. Хроматы – желтые кристаллические вещества – желтую окраску обеспечивает хромат-ион Сг042-. Дихроматы – соли дихромовой кислоты Н2Сг07. В отличие от хроматов, почти все соли-дихроматы хорошо растворимы в воде. Дихроматы имеют ярко-оранжевую окраску, обеспеченную дихромат-ионом: Сг072-.Хромат и дихромат-ионы способны к взаимопревращению в зависимости от кислотности среды: если раствор подкислить, то хромат-ионы будут переходить в дихромат-ионы по схеме:
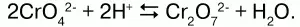
Если добавить щелочи, то пойдет обратная реакция:
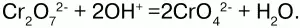
Хроматы получают взаимодействием оксида хрома (VI) или раствора хромовой кислоты H2CrO4 с оксидами, гидроксидами, карбонатами металлов или при обменной реакции с участием растворимых солей-хроматов, или путем окисления комплексных солей – гидроксохроматов в избыточном растворе щелочи:
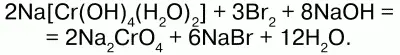
Хромат калия K2CrO 4– кристаллы желтого цвета, при нагревании краснеют. Кристаллогидратов не образует. Дихроматы – сильные окислители:
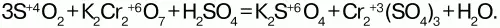
Получают дихроматы из соединений Cr (III) в кислой среде:
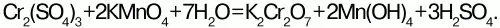
Дихромат аммония (NH4)2Cr2O7 –оранжевые кристаллы, не образует кристаллогидратов. При слабом нагревании он самовоспламеняется с выбросом искр – раскаленных частиц Cr2O3, N2 и паров воды – «химический вулкан».
Дихромат калия K2Cr2O7?2H2O и Na2Cr2O7– хромпики, оранжево-красные кристаллы, кристаллогидратов не образует. Используется в пиротехнике, в хроматометрии, в производстве спичек. Смесь равных объемов раствора K2Cr2O7 и концентрированной серной кислоты – хромовая смесь – является очень сильным окислителем, в лабораториях применяется для мытья стеклянной посуды. Хроматы применяются для протравы семян, при крашении, в лакокрасочной, кожевенной (в качестве дубящих реагентов кожи), текстильной промышленности; используются в лабораторном способе разделения хрома-тов кальция, стронция и бария.
Наиболее распространенным в природе, минералом является минерал PbCrO 4– крокоит. Хромат – тарапакаити дихромат калия – лопецит– также являются природными минералами.
66. Общая характеристика семейства железа
Семейство железавходит в состав побочной подгруппы восьмой группы и является в ней первой триадой, включающей в себя железо, кобальти никель. Эти элементы имеют два электрона на наружном слое атома, все они являются металлами. По свойствам все три элемента похожи между собой. Для них характерна степень окисления 2, 3, 4. Реже проявляются более высокие степени окисления. Ни один элемент из семейства железа не проявляет максимальной степени окисления +8. Все металлы триады образуют разнообразные соединения, проявляя степени окисления +2 и +3. Проявление высокой степени окисления и амфотерных свойств характерно для железа.
Читать дальше
Конец ознакомительного отрывка
Купить книгу