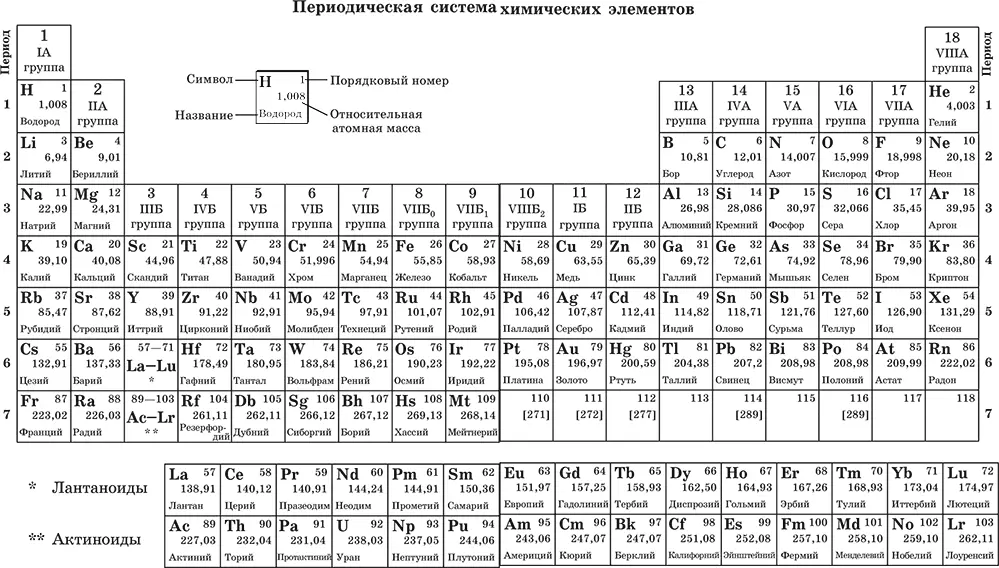
Проследим, например, изменение высших и низших степеней окисления у элементов IA – VIIA-групп во втором – четвертом периодах по табл. 3.
Положительные степени окисления проявляют все элементы, за исключением фтора. Их значения увеличиваются с ростом заряда ядер и совпадают с числом электронов на последнем энергетическом уровне (за исключением кислорода). Эти степени окисления называют высшими степенями окисления. Например, высшая степень окисления фосфора Р равна +V.

Отрицательные степени окисления проявляют элементы, начиная с углерода С, кремния Si и германия Ge. Значения их равны числу электронов, недостающих до восьми. Эти степени окисления называют низшими степенями окисления. Например, у атома фосфора Р на последнем энергетическом уровне недостает трех электронов до восьми, значит, низшая степень окисления фосфора Р равна – III.
Значения высших и низших степеней окисления повторяются периодически, совпадая по группам; например, в IVA-группе углерод С, кремний Si и германий Ge имеют высшую степень окисления +IV, а низшую степень окисления – IV.
Эта периодичность изменения степеней окисления отражается на периодическом изменении состава и свойств химических соединений элементов.
Аналогично прослеживается периодическое изменение электроотрицательности элементов в 1—6-м периодах IA– VIIA-групп (табл. 4).
В каждом периоде Периодической системы электроотрицательность элементов увеличивается при возрастании порядкового номера (слева направо).
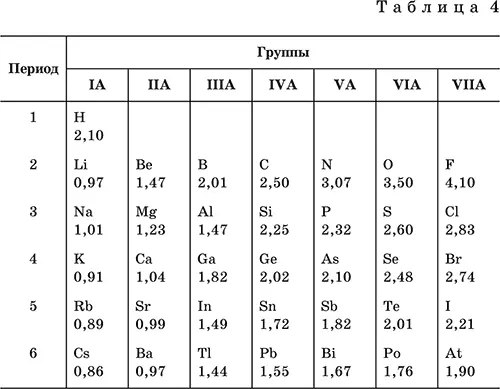
В каждой группеПериодической системы электроотрицательность уменьшается при возрастании порядкового номера (сверху вниз). Фтор F обладает наивысшей, а цезий Cs – наинизшей электроотрицательностью среди элементов 1—6-го периодов.
У типичных неметаллов – высокая электроотрицательность, а у типичных металлов – низкая.
Примеры заданий частей А, В
1.В 4-м периоде число элементов равно
1) 2
2) 8
3) 18
4) 32
2.Металлические свойства элементов 3-го периода от Na до Сl
1) силиваются
2) ослабевают
3) не изменяются
4) не знаю
3.Неметаллические свойства галогенов с увеличением порядкового номера
1) возрастают
2) понижаются
3) остаются без изменений
4) не знаю
4.В ряду элементов Zn – Hg – Со – Cd один элемент, не входящий в группу, – это
1) Са
2) Cs
3) Cd
4) Со
5.Металлические свойства элементов повышаются по ряду
1) In – Ga – Al
2) К – Rb – Sr
3) Ge – Ga – Tl
4) Li – Be – Mg
6.Неметаллические свойства в ряду элементов Аl – Si – С – N
1) увеличиваются
2) уменьшаются
3) не изменяются
4) не знаю
7.В ряду элементов О – S – Se – Те размеры (радиусы) атома
1) уменьшаются
2) увеличиваются
3) не изменяются
4) не знаю
8.В ряду элементов Р – Si – Аl – Mg размеры (радиусы) атома
1) уменьшаются
2) увеличиваются
3) не изменяются
4) не знаю
9.Для фосфора элемент с меньшейэлектроотрицательностью – это
1) N
2) S
3) Сl
4) Mg
10.Молекула, в которой электронная плотность смещена к атому фосфора, – это
1) PF 3
2) РН 3
3) P 2S 3
4) Р 2O 3
11. Высшаястепень окисления элементов проявляется в наборе оксидов и фторидов
1) СlO 2, РСl 5, SeCl 4, SO 3
2) PCl, Аl 2O 3, КСl, СО
3) SeO 3, ВСl 3, N 2O 5, СаСl 2
4) AsCl 5, SeO 2, SCl 2, Cl 2O 7
12. Низшаястепень окисления элементов – в их водородных соединениях и фторидах набора
1) ClF 3, NH 3, NaH, OF 2
2) H 3S +, NH+, SiH 4, H 2Se
3) CH 4, BF 4, H 3O +, PF 3
4) PH 3, NF+, HF 2, CF 4
13.Валентность для многовалентного атома одинаковав ряду соединений
1) SiH 4– AsH 3– CF 4
2) РН 3– BF 3– ClF 3
3) AsF 3– SiCl 4– IF 7
4) H 2O – BClg – NF 3
14.Укажите соответствие между формулой вещества или иона и степенью окисления углерода в них

3. Молекулы. Химическая связь. Строение веществ
Химические частицы, образованные из двух или нескольких атомов, называются молекулами (реальными или условными формульными единицами многоатомных веществ). Атомы в молекулах химически связаны.
Читать дальше
Конец ознакомительного отрывка
Купить книгу
















