Кроме активных форм кислорода, бета-амилоид отличается особой жестокостью и по отношению к бактериям. Налипая на их поверхность, он нейтрализует вещества, с помощью которых они отбиваются от иммунной атаки, и тем самым ускоряет их гибель. В мозге больных Альцгеймером нередко обнаруживают [374] Dominy S. S. et al. Porphyromonas gingivalis in Alzheimer's disease brains: Evidence for disease causation and treatment with small-molecule inhibitors // Science Advances. 2019 Jan; 5 (1): eaau3333.
микроба Porphyromonas gingivalis , поэтому некоторые ученые считают этих бактерий фактически возбудителями болезни. Свою лепту в образование амилоидных бляшек вносят и вирусы, в частности герпес. Несмотря на то что бета-амилоид никак не влияет на жизнь вирусных частиц, они могут становиться [375] Ezzat K. et al. The viral protein corona directs viral pathogenesis and amyloid aggregation // Nature Communications. 2019 May; 10: 2331.
центром его агрегации, поскольку на их поверхность всегда налипает множество внеклеточных белков.
Таким образом, запустить развитие болезни Альцгеймера может практически все что угодно. И поэтому еще одним важным фактором риска становится возраст. Чем дольше человек живет, тем больше шансов встретиться у АРР и β-секретазы. Так же можно объяснить и то, почему болезнью Альцгеймера чаще страдают женщины – они просто в среднем дольше живут.
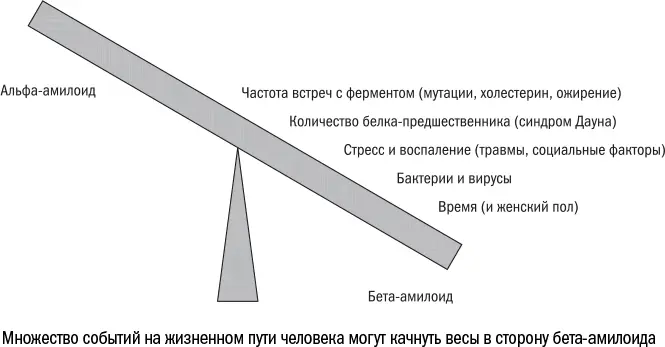
Чем больше времени проходит, тем выше вероятность, что в жизнь мозга вмешаются еще какие-нибудь события: травма, воспаление, стресс, заражение вирусом или размножение бактерий. Застраховаться от них невозможно, особенно учитывая, что многие из этих факторов риска очень распространены. Бактерия Porphyromonas , которая стала изначально известной благодаря вызываемому ей периодонтиту (воспалению связок, удерживающих зуб в десне), встречается [376] Griffen A. L. et al. Prevalence of Porphyromonas gingivalis and periodontal health status // Journal of Clinical Microbiology. 1998 Nov; 36 (11): 3239–3242.
у каждого четвертого человека в составе здоровой микрофлоры рта. А герпесом, по последним данных, заражены [377] Human Herpesviruses. Cambridge University Press, 2007.
около 70 % людей. С этой точки зрения в зоне повышенного риска развития болезни Альцгеймера оказывается почти каждый из нас. И когда мы начинаем искать пути ее лечения, ситуация становится еще сложнее.
Подкрадываться к многоликому и неуловимому противнику можно с разных сторон. Одна стратегия – поразить его на подходе, еще до того, как начнется гибель нервных клеток. Здесь могла бы помочь, например, генная терапия: можно было бы вырезать у пациентов "рискованные" варианты гена АРОЕ . Другой вариант – уничтожать патогенов, которые провоцируют выделение амилоида, вроде Porphyromonas gingivalis . Первый метод еще находится в разработке, второй уже тестируют на пациентах с мягкой формой болезни Альцгеймера.
Но можно зайти и с другого конца и бороться с последствиями, раз уж мы не можем предугадать возникновение болезни. Так, собственно, и действуют современные лекарства от болезни Альцгеймера: они не предотвращают гибель клеток и дегенерацию, а лишь смягчают симптомы. Аналогичный подход пытается разработать Тони Висс-Кори, который начал тестировать переливание больным плазмы крови от молодых доноров в надежде на то, что GDF11 или какие-то другие "молодящие" вещества заставят нервные клетки больных размножаться. Наконец, можно бороться непосредственно с амилоидом, так или иначе настраивая против него иммунную систему, например вакцинируя пациентов его фрагментами.
Тем не менее ни один из этих подходов пока не сработал до конца. Многие компании, занимающиеся разработкой лекарств (в том числе крупнейшие – Merck, Pfizer, Roche), уже капитулировали перед врагом. На плаву держатся лишь небольшие стартапы, чьи продукты, впрочем, пока не вышли за пределы клинических испытаний. В чем же проблема? Пусть мы не воссоздали пока подробную картину заболевания, но все же примерно представляем куда стрелять. Почему мы допускаем осечку за осечкой? Одно из возможных объяснений состоит в том, что у болезни Альцгеймера слишком много причин. Удаляя амилоид, мы не мешаем его накоплению. Сражаясь с бактериями, мы упускаем из вида вирус герпеса и холестерин. Но как одним ударом обрубить все головы этой гидры?
Важный шаг в этом направлении сделал американский врач Дейл Бредесен, автор книги "Нестареющий мозг" (The end of Alzheimer's, дословно "Конец Альцгеймера") [378] Бредесен Д. Нестареющий мозг. – М.: Эксмо, 2019.
. Он предположил, что болезнь Альцгеймера – это несколько разных патологий с общими проявлениями. Бредесен разработал свою методику, согласно которой необходимо сначала определить, каким именно типом болезни страдает пациент: вызвана ли она стрессом, воспалением или дистрофией (истощением пула клеток) нервной ткани. В зависимости от этого Бредесен предлагает выбрать протокол лечения, чтобы устранить причину болезни данного конкретного пациента. Группа, которая работала по этой методике, уверяет [379] Bredesen D. E. et al. Reversal of cognitive decline: 100 patients // Journal of Alzheimer's disease & Parkinsonism. 2018; 8: 5.
, что смогла обратить вспять деменцию у сотни пациентов. Впрочем, клинических испытаний эта терапия еще не прошла, поэтому говорить о ее эффективности пока рано.
Читать дальше
Конец ознакомительного отрывка
Купить книгу













