Лит. см. при ст. Цианиды.
Циана'ты,соли и эфиры циановой кислоты. Соли, в отличие от самой кислоты, соединения весьма устойчивые; например, для NaOCN t пл 550 °С; KOCN разлагается, не плавясь, лишь при температуре 700 °С.
Ц. щелочных металлов растворимы в воде, не растворимы в спирте и эфире; их получают окислением соответствующих цианидов (кислородом воздуха, окислами свинца PbO, PbO 2и др.) и применяют в различных синтезах, например для получения семикарбазида. Аммониевая соль NH 4OCN, на примере которой Ф. Вёлер (1828) впервые осуществил синтез органического вещества (мочевины) из неорганического, может быть получена обменной реакцией из Ц. серебра и хлорида аммония.
Эфиры циановой кислоты существуют в двух изомерных формах: ROCN и RNCO. Цианаты ROCN практического значения не имеют. Изоцианаты RNCO применяются в промышленности для производства полиуретанов, гербицидов.
Лит. см. при ст. Цианиды.
Циангидри'ны,a-оксинитрилы, нитрилы a-оксикислот, органические соединения, содержащие окси- и цианогруппу у одного атома углерода,
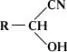 (см. Оксинитрилы ) .
(см. Оксинитрилы ) .
Циане'и(ботанические), то же, что синезелёные водоросли.
Циане'я(Cyanea capillata), крупная морская медуза из класса сцифоидных. Края зонтика с восемью двойными лопастями, щупальца собраны в 8 пучков. Окраска тела обычно очень яркая, зонтик желтовато-красный, ротовые лопасти малиновые, щупальца розовые. Диаметр зонтика от нескольких см до 2 м, щупальца достигают в вытянутом состоянии 40 м . На щупальцах большое кол-во стрекательных клеток, служащих для нападения и защиты (между щупальцами Ц. обычно держатся мальки пикши и некоторых др. тресковых рыб, находящие здесь защиту). Обитают Ц. в сев. частях Атлантического и Тихого океанов и в морях Северного Ледовитого океана.

К ст. Цианея.
Циани'д ка'лия,цианистый калий, KCN. Бесцветные гигроскопичные кристаллы, t кип 635 °С, плотность 1,56 г/см 3 (25 °С). Хорошо растворим в воде (41,7% при 25 °С, 55% при 103,3 °С). В водном растворе гидролизуется с выделением HCN; константа гидролиза 2,54×10 -5(25 °С), Проявляет большую склонность к образованию комплексных соединений, например калия гексацианоферроата.
В промышленности Ц. к. получают главным образом нейтрализацией HCN гидроокисью калия КОН. О применении Ц. к. см. Цианиды. Ц. к. очень токсичен. О действии на организм и о технике безопасности при работе с ним см. Синильная кислота.
Лит. см. при ст. Цианиды.
Циани'д на'трия,цианистый натрий, NaCN. Бесцветные гигроскопичные кристаллы; t пл 564 °С; плотность 1,5955 г/см 3 (20 °С). Кристаллизуется в виде NaCN×2H 2O, выше 34,7 °С — в безводной форме. Хорошо растворим в воде (32,4% при 10 °С, 45,0% при 35 °С). В водных растворах гидролизуется:
NaCN + H 2O Û HCN + NaOH.
Как и KCN, Ц. н. легко образует комплексные соединения. В промышленности Ц. н. получают главным образом нейтрализацией синильной кислоты гидроокисью натрия NaOH. О применении Ц. н. см. Цианиды. Ц. н. очень токсичен. О действии на организм и мерах предосторожности при работе с ним см. Синильная кислота.
Лит. см. при ст. Цианиды.
Циани'ды,соли синильной кислоты. Ц. щелочных металлов MeCN и щёлочноземельных металлов Me (CN) 2(где Me — металл) термически устойчивы, в водных растворах гидролизуются. Ц. тяжёлых металлов термически неустойчивы, в воде, кроме Hg (CN) 2, нерастворимы. При окислении Ц. образуют цианаты (например, 2KCN + O 2® 2KOCN). Многие металлы при действии избытка цианида калия или цианида натрия дают комплексные соединения, что используется, например, для извлечения золота и серебра из руд (см. Цианирование ) :
4NaCN + 2Au+ 1/ 2O 2+ H 2O ® 2Na [Au (CN) 2] + 2NaOH.
Золото и серебро из раствора выделяют электролитическим осаждением либо при действии металлического цинка. Растворы цианидных комплексов золота, серебра, цинка и др. металлов используют в гальванотехнике для получения покрытий. Ц. применяют в органическом синтезе, например для получения нитрилов, в качестве катализатора (см. Бензоиновая конденсация ) . Ц. очень токсичны. О действии на организм и мерах предосторожности при работе с Ц. см. Синильная кислота.
Читать дальше

 (см. Оксинитрилы ) .
(см. Оксинитрилы ) .