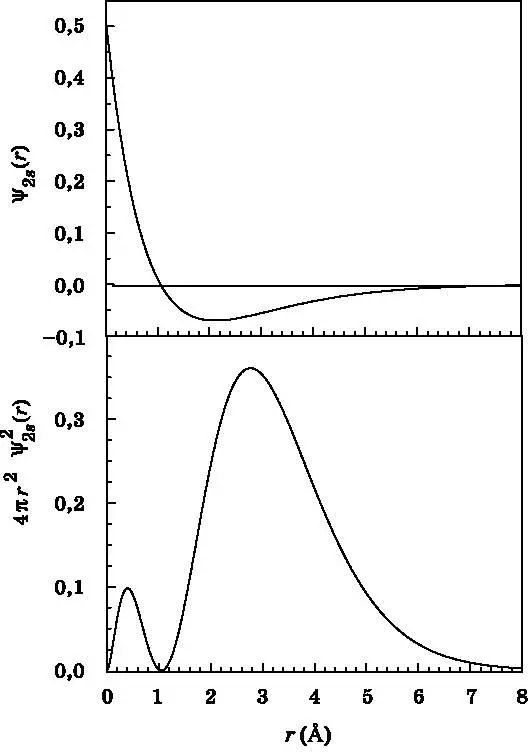
Рис. 10.5. Волновая функция (вверху) и функция радиального распределения (внизу) для 2s-орбитали атома водорода в зависимости от расстояния rдо протона. Волновая функция начинается с положительного значения, проходит через узел чуть дальше точки 1 Å (2 a 0 ) и затем спадает до нуля. Функция радиального распределения демонстрирует максимум вероятности обнаружения электрона на отметке 2,8 Å, причём наиболее вероятно найти его в интервале от 2 до 4 Å (см. рис. 10.2). Расстояние rизмеряется в ангстремах (1 Å = 10 −10 м)
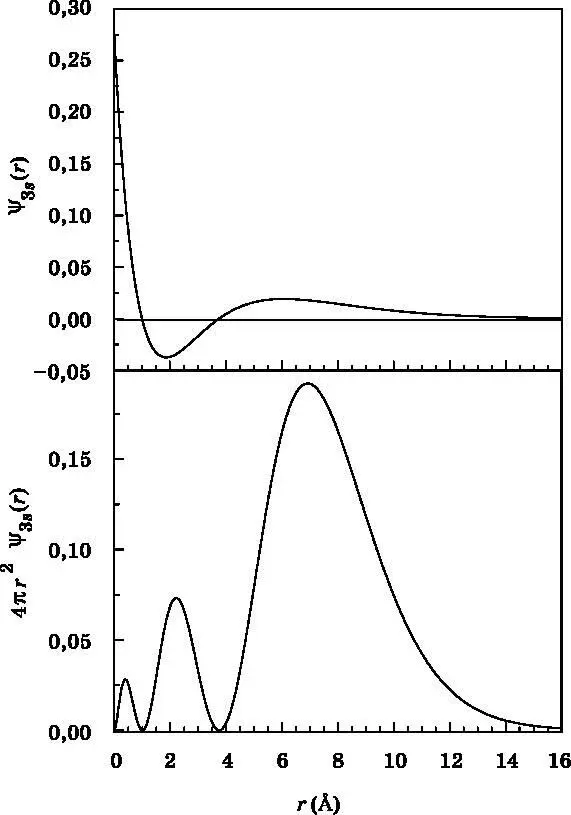
Рис. 10.6. Волновая функция (вверху) и функция радиального распределения (внизу) для 3s-орбитали атома водорода в зависимости от расстояния rдо протона. Волновая функция начинается с положительного значения, проходит через узел, становясь отрицательной, проходит через второй узел, вновь становясь положительной, и затем спадает до нуля. Функция радиального распределения показывает, что вероятность обнаружения электрона достигает максимума на отметке 7 Å, причём наиболее вероятно найти его в интервале от 5 до 11 Å (см. рис. 10.2). Расстояние rизмеряется в ангстремах (1 Å = 10 −10 м)
Как уже подробно говорилось, волновые функции — это волны амплитуды вероятности. Подобно другим волнам, они могут быть положительными и отрицательными. В нижней части рис. 10.5 показана функция радиального распределения для состояния 2 s . Это вероятность обнаружить данный электрон на расстоянии r от ядра. Вероятности всегда имеют положительные значения, поскольку являются квадратами волновой функции, которые всегда положительны.
Волна может быть положительной или отрицательной, но имеющие смысл значения вероятности являются положительными числами или нулём. Функция радиального распределения показывает, что бо́льшая часть вероятности приходится на интервал от 2 до 4 Å; это также видно на рис. 10.2, но без количественного описания. Пик вероятности приходится на отметку приблизительно 2,8 Å.
Из рис. 10.6 видно, что волновая функция 3 s -орбитали имеет два узла, то есть дважды пересекает ноль. В этом отношении волновые функции атома водорода подобны волновым функциям частицы в ящике (см. рис. 8.4). При n =1 узлов нет. При n =2 имеется узел. При n =3 имеется два узла. Число узлов для s -орбиталей равно n −1. Волновая функция 3 s начинается с положительного значения, затем становится отрицательной, а потом вновь положительной. В конце концов она спадает до нуля, становясь очень малой за отметкой 16 Å. Функция радиального распределения для 3 s -орбитали показывает, что область наибольшей вероятности обнаружить электрон находится относительно далеко от ядра. Пик вероятности расположен приблизительно на 7 Å, а на интервал от 5 до 11 Å приходится наибольшая вероятность найти электрон. Три функции радиального распределения, изображённые на рис. 10.4–10.6, дают количественное выражение для информации, схематически представленной на рис. 10.2. По мере увеличения главного квантового числа ( n ) s -орбитали становятся больше и количество узлов возрастает.
Для 2 s -орбитали n =2, l =0 и m =0. Однако при n =2 число l также может быть равно 1 и с ним могут быть связаны три значения m : m = 1, 0, −1. Эти три значения m соответствуют трём различным 2 p -орбиталям. Они показаны на диаграмме энергетических уровней на рис. 10.1.
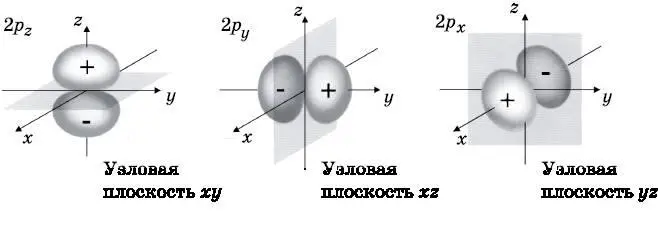
Рис. 10.7. Схематическое изображение трёх 2p-орбиталей атома водорода: 2p z , 2p y и 2p x . У каждой из них имеется два лепестка: один положительный и один отрицательный. У каждой есть узловая плоскость, то есть плоскость, где вероятность обнаружить электрон равна нулю. Лепестки 2p z -орбитали располагаются вдоль оси z, а узловой является плоскость xy, выделенная серым тоном. У 2p y -орбитали лепестки расположены вдоль оси y, а основная плоскость — в плоскости xz. Лепестки 2p x -орбитали лежат вдоль оси z, а узловая плоскость — это yz. Лепестки на этой схеме показывают, где находится область с максимальной амплитудой вероятности для электрона. Волны амплитуды вероятности плавно спадают к нулю вдали от ядра (протона), а не обрываются резко, как на этих диаграммах
Читать дальше















