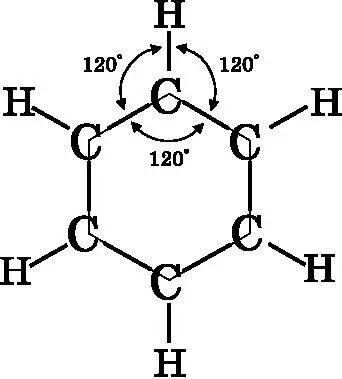
Рис. 18.1. Геометрия молекулы бензола C 6 H 6 . Бензол имеет форму правильного плоского шестиугольника
Где находятся двойные связи?
На рис. 18.2 изображены две возможные структуры с двойными связями. В обоих случаях каждый атом углерода образует четыре связи. Углерод образует три σ-связи — одну с водородом и по одной с двумя соседними атомами углерода. Каждый атом углерода участвует в двойной связи с одним из соседних атомов углерода. Диаграммы, изображённые справа и слева, идентичны, за исключением расположения двойных связей.
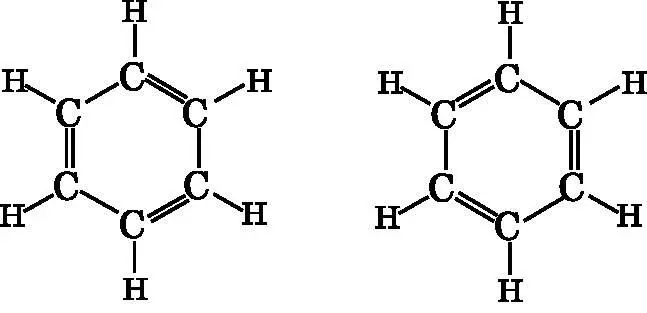
Рис. 18.2. Две возможные конфигурации двойных связей в бензоле. В обеих все атомы углерода образуют по четыре связи
Два момента, относящиеся к связям в молекуле бензола, отражены на рис. 18.2 неверно. При обсуждении двойных связей в главе 14 была приведена табл. 14.1, из которой видно, что двойные углерод-углеродные связи значительно короче одиночных. Двойная связь в этилене имеет длину 1,35 Å против 1,54 Å для одиночной связи в этане. Так что если в бензоле двойные и одиночные связи чередуются, то в нём должны чередоваться короткие и длинные углерод-углеродные звенья. Однако эксперименты убедительно показывают, что бензол является правильным шестиугольником и все углерод-углеродные связи в нём имеют одинаковую длину.
Если закрыть глаза на то, что диаграмма подразумевает неравную длину связей, то вторая проблема состоит в выяснении, какая из двух диаграмм верна — правая или левая? Нет никаких причин предпочесть одну другой. В первых попытках объяснения предполагалось, что связи постоянно переключаются между конфигурациями на правой и левой диаграммах. В результате такого перескакивания получается своего рода усреднённая структура. Эта идея является шагом в правильном направлении, но подлинный ответ, который впоследствии оказался применимым ко многим типам систем, касается природы образующихся молекулярных орбиталей.
На рис. 18.3 схематически изображены атомные орбитали, участвующие в образовании молекулярных орбиталей бензола. Сверху нарисованы гибридные атомные орбитали, служащие для создания σ-связей. Каждый атом углерода использует три гибридные sp 2-орбитали для образования трёх σ-связей — одной с атомом водорода и по одной для двух соседних атомов углерода. Образование этих трёх sp 2-гибридизированных атомных орбиталей оставляет каждому атому углерода по одной избыточной p -орбитали. В верхней части рис. 18.3 за плоскость xy принята плоскость, содержащая атомы (плоскость страницы). Тогда у каждого атома углерода остаётся неиспользованная p z-орбиталь, расположенная перпендикулярно плоскости страницы. Эти орбитали изображены в нижней части рисунка. Положительные и отрицательные лепестки орбиталей расположены над и под плоскостью кольца. На этой диаграмме длина связи между атомами углерода преувеличена, а ширина p z-орбиталей приуменьшена, чтобы сделать изображение более понятным. В действительности же p z-обитали перекрываются, что в более реалистичных пропорциях показано на рис. 14.15.
Эти шесть атомных p z-орбиталей объединяются и образуют молекулярные орбитали. Без нарушения принципа Паули эти атомные орбитали могут содержать максимум 12 электронов. Поэтому шесть атомных орбиталей образуют суперпозицию и дают шесть молекулярных орбиталей (МО), которые также могут вмещать максимум 12 электронов. Эти МО не связаны с конкретным атомом или даже конкретной парой атомов. Они растянуты на всю систему из шести атомов углерода.
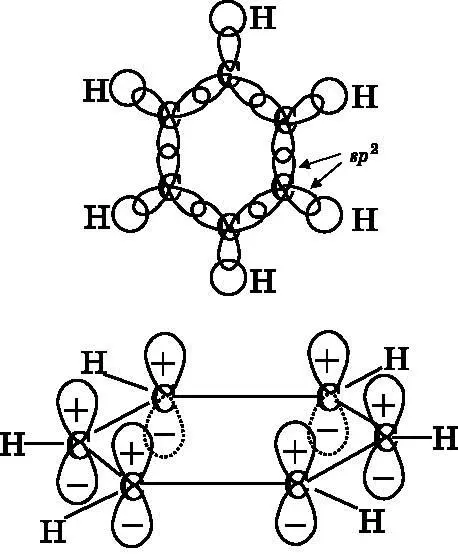
Рис. 18.3. Вверху: бензол и σ- связи. Каждый атом углерода образует три связи, используя три sp 2 -орбитали, лежащие в плоскости xy. У каждого атома углерода остаётся pz-орбиталь, перпендикулярная плоскости бензольного кольца. Внизу: p z -орбитали углерода имеют положительные и отрицательные лепестки, которые расположены над и под плоскостью кольца. Длина связей здесь преувеличена, а ширина лепестков, наоборот, приуменьшена для того, чтобы иллюстрация стала понятнее. Лепестки соседних p z -орбиталей перекрываются
Читать дальше















