Сен Гук Ким, Ирина Сенгуковна Ким, Дмитрий Сенгукович Ким
Элементы
«Всё сущее есть число»
Пифагор
Пифагор не только к тексту, но и к тесту. Тесту на математичность окружающего Мира, Вещественного Мира из химических элементов. Химические элементы – числа: номера химических элементов; числа электронов и нуклонов в атомах химических элементов; квантовые числа… Вся материя в Вещественном Мире из химических элементов: атомы, молекулы, наночастицы, тела, газопылевые туманности, небесные тела, скопления галактик…. Всё (на сегодня) множество химических элементов, составляющих 118 номеров, традиционно распределяют в Периодических Таблицах. Исходя из своих таблиц, известных на то время химических элементов, Д. И. Менделеев открыл Периодический Закон. Но этот фундаментальный Закон Природы оформлен только таблично, сформулирован только словесно, и не имеет математических формул. Таблицы без формул – числовые шифры без ключей. Математические формулы – ключи к числовым шифрам.
В более чем двухвековой истории систематизации химических элементов наибольших успехов в XIX веке достигли британец Джон Александр Ньюлендс, германец Юлиус Лотар Мейер и россиянин Дмитрий Иванович Менделеев. В последней прижизненной Таблице Менделеева было IX групп:
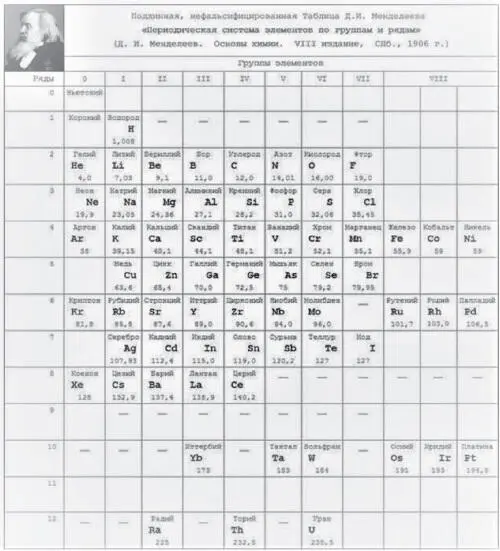
Рис. 1. Последняя прижизненная Периодическая Таблица Д.И. Менделеева
Как видно на рис. 1, у Менделеева была нулевая группа элементов, которая содержала доводородные элементы под номером, очевидно, 0 – Ньютоний (эфир), а под номером 1 – Короний. Водород, по-видимому, имел номер 2, Гелий – номер 3…., и т. д. Дмитрий Иванович почему-то не ставил номера элементам, видимо, полагая это очевидным по порядку расположения элементов в его Периодической Таблице: слева направо в рядах (писал и говорил именно о рядах, а не о периодах) и сверху вниз самих рядов (периодов). В восьмой (девятой от нулевой) группе были только триады: Fe, Со, Ni; Ru, Rh, Pd; Os, Ir, Pt.
Музыкальная октавная гармония, воплощённая в «Законе октав» Ньюлендса в его систематизации химических элементов, имела столь завораживающее воздействие на людей, что 120 лет после открытия Менделеевым Периодического Закона в Мире пользовались Периодической Таблицей химических элементов из VIII гомологических групп элементов-аналогов. В постменделеевский период вплоть до 1989 г. наиболее популярной и повсеместно используемой была Периодическая Таблица вида:
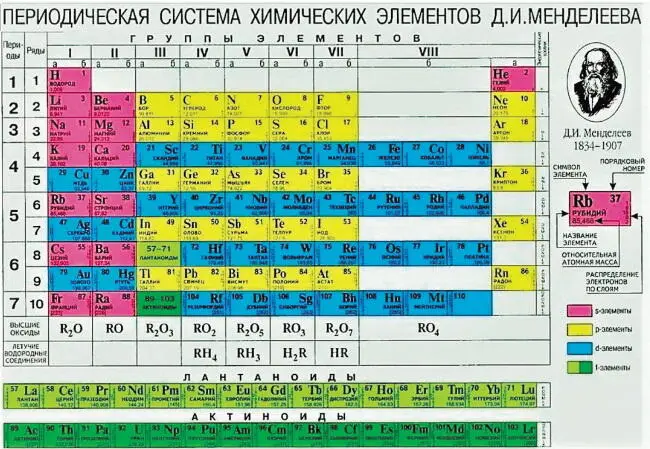
Рис. 2. Наиболее распространённая форма Периодической Таблицы химических элементов до 1989 г.
По сравнению с последней прижизненной Периодической Таблицей Менделеева нулевой группы вместе с нулевым элементом, Коронием и инертными элементами нет, первый номер у Водорода, Гелий и инертные газы из бывшей нулевой группы перенесены в группу VIII, где размещены и триады благородных металлов. Гелий поднялся на один ряд выше и стоит номером 2 в одном ряду с Водородом через 6 групп в крайней правой главной подгруппе VIII группы.
Размещение Гелия над Неоном и другими инертными газами было вполне понятно и оправдано во времена Менделеева, когда не знали о строении атомов, и не было квантовой механики. В самом деле, газ Гелий более инертен, чем все другие благородные газы и имеет наименьшую атомную массу среди них. Поэтому логично было ставить Гелий на первое место типозадающего элемента в гомологической группе инертных атомарных элементов-аналогов.
Но, когда открыли строение атомов, и было установлено, что в явлении периодичности свойств химических элементов лежит квантово-механическая основа формирования электронных оболочек, становится непонятным положение Гелия на рис. 2. Это в таблицах из VIII групп. Но, такая же картина сохраняется и в современных, после 1989 г., типах Периодических Таблиц с 18-ю группами.

Рис. З.Периодическая Таблица химических элементов с 18-тью группами, рекомендуемая IUPAC с 1989 г.
Уже с беглого взгляда на рис. 2 и рис. З отчётливо видно, будто Гелий вырван из естественного положения рядом с Водородом и перекинут на самую правую и верхнюю позицию над Неоном. При этом на обоих рис. 2 и 3 видно, что ячейка с Гелием, по цвету такая же, как у двух групп s-элементов. Как s-элемент Гелий может быть типозадающим в группе p-элементов? Авторы этих Таблиц, по-видимому, таким вопросом не задавались. Если же задавались, то предпочли не выходить за рамки сложившихся в XIX веке традиций. А, ведь, Таблицы на рис. 2 и рис. 3 создавались в середине XX века, когда строение атомов и формирование электронных оболочек на квантово-механической основе были повсеместно признаны и приняты.
Читать дальше















