Ковалентная связь осуществляется посредством обобществления двух валентных электронов (по одному от каждого из двух соседних атомов в молекуле). Пара обобществленных электронов принадлежит одновременно двум атомам молекулы. Электроны, образующие связь, стремятся к частичной локализации в пространстве между двумя атомами, соединенными этой связью. В этом смысле ковалентная связь характеризуется явно выраженным свойством направленности. Это хорошо видно на примере молекулы метана CH 4(рис. 1). У атома углерода четыре валентных (внешних) электрона, а каждый из атомов водорода имеет один электрон. Эти восемь электронов сосредоточены главным образом вдоль прямых, соединяющих протоны (ядра атома водорода) с ядром атома углерода.
К образованию ковалентных связей имеют тенденцию атомы III, IV и V групп периодической системы элементов. Так, углероду, кремнию и германию не хватает четырех электронов до заполнения их электронных оболочек, и поэтому атомы этих элементов могут притягиваться в основном за счет перекрытия оболочек. К веществам с ярко выраженной ковалентной связью относятся кристаллы алмаза, кремния, карбида кремния, арсенида галлия и др.
Если кристаллы с ковалентным и ионным типами связи рассматривать как предельные случаи, то между ними имеется ряд кристаллов, обладающих промежуточными типами связи.
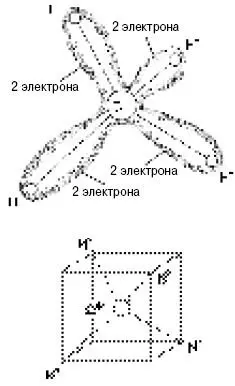
Рис. 1.Геометрия молекулы метана. Ядра водорода расположены в вершинах правильного тетраэдра, или в четырех из восьми вершин куба. Электроны сконцентрированы вдоль прямых «углерод – водород»
37. МЕТАЛЛИЧЕСКАЯ СВЯЗЬ. СВЯЗЬ ВАН ДЕР ВААЛЬСА
Металлическая связь реализуется в кристаллах различных металлов и не имеет аналога в двухатомных молекулах. В металлических кристаллах атомы расположены настолько близко, что волновые функции внешних электронов существенно перекрываются. Вследствие этого валентные электроны получают возможность переходить от одного атома к другому и могут довольно свободно перемещаться по всему объему кристалла. Таким образом, валентные электроны в металле нельзя считать связанными с одним или несколькими ионами металла, они являются общими для всего объема металла. Поэтому валентные электроны в металлах принято называть «обобществленными» или «коллективизированными».
Свободно перемещающиеся электроны в металле во многом напоминают молекулы газа, находящегося в сосуде. Поэтому для обозначения совокупности свободных валентных электронов внутри металлического кристалла используется термин «электронный газ». Электронный газ, несущий отрицательный заряд, связывает в прочную систему положительно заряженные ионы металла. Без «цементирующего» действия электронного газа одноименно заряженные ионы металла должны были бы удаляться друг от друга под действием кулоновских сил отталкивания, что привело бы к разрушению кристалла. Таким образом, под влиянием двух противоположных сил – «стягивающего» действия коллективизированных электронов и сил отталкивания между ионами – последние располагаются на определенном расстоянии друг от друга, соответствующем минимуму энергии системы.
Связь Ван дер Ваальса – это связь между атомами или молекулами, обусловленная взаимодействием их электрических дипольных моментов. Вандерваальсовы силы взаимодействия возникают между полярными молекулами, обладающими постоянными дипольными моментами (такими как H 2O, HCl и т. д.), за счет поляризации неполярных молекул полярными, а также за счет создания мгновенных дипольных моментов. Мгновенные дипольные моменты создаются благодаря тому, что электроны и ядра в атомах и неполярных молекулах находятся в постоянном движении. Вследствие этого центры отрицательных и положительных зарядов, вообще говоря, не совпадают. В результате создается мгновенный дипольный момент в атоме или молекуле, который своим электрическим полем поляризует соседний атом или молекулу, а это означает появление второго диполя. Взаимодействие диполей приводит к сближению атомов или молекул, в результате электронные оболочки начинают перекрываться и взаимодействовать, что приводит к появлению сил отталкивания, компенсирующих силы притяжения. Это создает условия образования кристаллов из нейтральных атомов (например, из инертных газов) или неполярных молекул.
Читать дальше
Конец ознакомительного отрывка
Купить книгу