Смотришь на ветку или пень, а они будто под снегом. Под подводным снегом!
Может быть, все-таки вечная мерзлота виной всему, она как-то переохлаждает реку…
Нет… Не всюду на реке всплывают осенние льдины, а мерзлота — всюду. И «подводный снег» тоже не везде на Севере увидишь.
Конечно, влияние мерзлоты сказывается. Не будь ее, не было бы и осеннего ледохода. На южных реках его поэтому и нет. Скорее всего, мерзлота усиливает какие-то естественные процессы в реке, которые, видимо, протекают и в несеверных реках, но протекают там слабо, почти незаметно.
Какие же это процессы? Или процесс?. Пожалуй, все-таки процесс! Фазовый переход. Ледообразование. Мерзлота убыстряет его. Поэтому мы видим осенние льдины на северных реках и не видим их на южных. Там, на юге, «осенний ледоход» начинается позже, идет подо льдом, он скрыт от взоров наблюдателя, но внутриводный лед, как известно, встречали там тоже. В Ленинграде, например.
Однако на главный вопрос ответа найти так и не удавалось. Не удавалось без предположения, вернее, без допущения: а что если в составе речной воды в малых количествах находится какая-то другая вода. Та, которая намораживается именно у дна и больше нигде. Известно ж, что все тяжелые частички в воде всегда стремятся вниз, ко дну, так велят им силы гравитации, силы тяжести… Тяжелая вода? А почему бы и нет.
Тяжелая вода — это изотопная разновидность обычной воды. Вместо обычного водорода (протия) здесь присутствует его изотоп — дейтерий, он вдвое тяжелее.
Всего же известны десятки изотопных разновидностей воды. Они очень существенно различаются между собой. Доказано, что теоретически возможно встретить в природе даже сотни «сортов» воды. Но это только теоретически. Не все изотопы водорода и кислорода пока известны науке, тем более что некоторые из них очень недолговечны.
Как считают ученые, например академик И. В. Петрянов-Соколов, у водорода может быть пять изотопов, ныне же известны лишь два — дейтерий и тритий. И оба они получаются из протия.
Поэтому известны протиевая, или обычная, дейтериевая, или тяжелая, вода, а также тритиевая, или сверхтяжелая, вода. Но тритий в природе очень редок, он не стабильный изотоп, поэтому сверхтяжелой воды почти не бывает. По одним расчетам выходит, что ее может быть всего несколько литров на планете, а по другим — несколько наперстков. В общем, не известно сколько.
Хотя по наблюдениям метеорологов замечено, что трития в природе прибавилось, особенно в 50-х годах, когда весьма часто в атмосфере испытывались различного вида атомные вооружения. Но этот тритий был все же не природного, а техногенного, искусственного, происхождения, как следствие повышенной радиации атмосферы.
Надо заметить, что природные дейтерий и тритий получаются из протия тоже под воздействием радиации, но только естественной или космической. Нейтрон космического происхождения, попадая в протиевую среду, может быть захвачен атомом протия… Конечно, процесс этот сложный, его изучает физика элементарных частиц, но упрощенно он выглядит именно так.
С нейтроном космического происхождения атом протия становится тяжелее, и с этого момента он уже называется дейтерием. Если к нему попадет еще один нейтрон, то, очевидно, атом станет еще тяжелее, и называться он уже будет тритием. Атомная масса у протия 1, у дейтерия 2, у трития 3.
Мировой океан, ледники, атмосферная влага — вот природные «фабрики тяжелой и сверхтяжелой воды». «Фабрики», которые работают без выходных — каждый год, каждый час, каждый миг.
Если мы откроем водопроводный кран, то там никогда не будет однородной воды — всегда только «разноизотопная» ее смесь. Причем молекул, содержащих дейтерий D 2O и HDO, окажется очень немного, по массе где-то 150 граммов в пересчете на тонну простой воды… Получается, что тяжелая вода есть всюду — в каждой капле, в каждой луже! — проблема в том, как ее взять.
150 граммов в пересчете на тонну. А много это или мало? И вообще, как оценивать подобные соотношения? 0,015 % — цифра явно невелика, чтобы говорить о ее весомости. И тем не менее. Для ее «прочувствования» проведем простейший опыт. В стакан с водой бросим несколько крупичек марганцовки, вообразив при этом, что марганцовка имитирует вкрапления тяжелой воды… Очень наглядный получается опыт. Вся вода окрашивается. А ведь несколько крупиц — это еще далеко не 0,015 %.
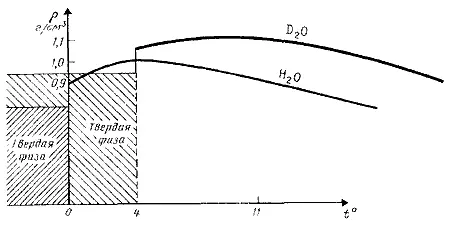
Рис. 4. Зависимость между температурой и плотностью протиевой и дейтериевой воды
Читать дальше











