Из лабораторных животных к болезни чувствительны белые мыши, морские свинки и кролики. При их искусственном инфицировании болезнь протекает в виде септицемии и через 24–72 ч наступает смерть. Обычно через 24 ч погибают белые мыши, а морские свинки и кролики — через 2–4 сут, иногда на 5–7 сут.
Белые крысы невосприимчивы к сибирской язве, но инбредные крысы линии Фишер-344 и Вистар чувствительны к токсину В. anthracis. К парентеральному введению В. anthracis чувствительны сирийские золотистые хомячки, суслики, хорьки.
Инфицирующие дозы для животных и людей.Обобщены в работе Н. В. Литусова с соавт. (2002). Величина ингаляционно поражающей дозы (Lct 50) для человека составляет около 20×10 3спор, a Lct 50при объеме дыхания человека 10 л/мин — 20×10 3спор×мин×л -1. Ингаляционные LD 50для морских свинок — 7,75×10 4, кроликов — 14×10 4, обезьян — 2,24×10 4, овец — 1,68×10 4, собак — 2,21×10 7, лошадей — 8×10 6спор. Величина LD 50для споровой культуры обычно на порядок больше для вегетативных клеток. Восприимчивость человека к ингаляционному поражению сибирской язвой ближе к восприимчивости кроликов, обезьян и овец, которые являются наиболее чувствительными к ингаляционному и подкожному заражению возбудителем сибирской язвы.
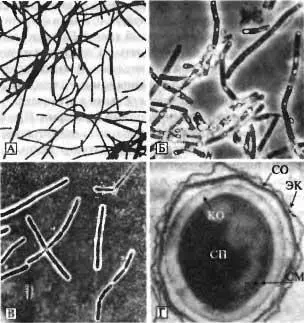
Рис. 3.2. Микроскопическое изображение В. anthracis. А. Микроскопическая картина клеток В. anthracis, штамм 14/41 в окрашенных мазках культур, выращенных на агаре Хоттингера в течение 24 ч и хранившихся при температуре 0–4 °C 96 ч. Увеличение 1150 раз. Целые клетки окрашены грамположительно (фиолетовый или черно-фиолетовый цвет), визированные клетки выглядят как грамотрицагельные (розового цвета). Б. Прижизненная микроскопическая картина клеток возбудителя сибирской язвы (штамм 4–7), выращенных на агаре Хоттингера в течение 24 ч. Иммобилизация клеток агаровым гелем. Фазовый контраст Увеличение: 1350 раз. Споры светлые и овальные. Бациллы темные, имеют форму удлиненных цилиндров, расположены поодиночке, попарно или соединены в цепочки. Внутри клеток мелкие светящчеся гранулы липидов и крупные, ярко блестящие споры. Лизирующиеся бациллы отличаются пониженной оптической плотностью цитоплазмы В Капсула живых сибиреязвенных бацилл штамма 4–7. Бациллы выращены на бикарбонатном агаре в атмосфере углекислого газа в течение 48 ч Влажный тушевой метод Фа ювый контраст. Увеличение: 1350 раз. Капсула препятствует проникновению туши к клеткам и по этой причине выглядит в виде ореола, окружающего бациллы Г. Зрелая спора В. anthracis, штамм 14/41 при электронной микроскопии. У зрелой споры кортекс электронно-прозрачный Компоненты спор СП — спороплазма; КО — кортекс; СМ — споровая мембрана; СО — споровая оболочка; ЭК — экзоспориум. По А. Г. Золотареву с соавт. (2006)
При алиментарном заражении LD 50 В. anthracis для животных, установленные опытным путем, составляли: для морских свинок — 1,62×10 8(1,49×10 8—1,76×10 8), кроликов — 3,93×10 8(3.5×10 8—4,4×10 8), обезьян — 2,05×10 7(1,6×10 7—2,6×10 7) и овец — 5×10 7спор. Расчетная LD 50для человека — 1,25×10 7спор В. anthracis.
Иммунитет.Лица, перенесшие сибирскую язву, приобретают стойкий, но не абсолютный иммунитет. Известны случаи повторного заболевания кожной формой сибирской язвы через 2 года (Никифоров В. Н., 1973).
Происхождение и молекулярная эпидемиология возбудителя сибирской язвы.Внутри рода Bacillus, возбудитель сибирской язвы относится к группе В. cereus, включающей шесть видов бацилл: В. cereus, В. thuringiensis, В. anthracis, В. weihenstepha.unsis, В. mycoides и В. Dseudomytoides. Патологические процессы у людей вызывают В. cereus и В. anthracis (Klee S. К. et al., 2010). До работы A. R. Hoffmaster et al. (2004) считалось, что В. cereus причастен только к пищевой токсикоинфекции и в затруднительных случаях его можно отличить от сибиреязвенного микроба по наличию у последнего плазмид pXO1 и рХО2. Однако эти авторы описали изолят бациллы, не являющейся В anthracis, но обладающей генами сибиреязвенного токсина и способной вызывать ингаляционное поражение у A/J-мышей, патоморфологически очень похожее на ингаляционную сибирскую язву. Фенотипически и по результатам 16S rRNA-анализа микроорганизм идентифицирован как цереус (В. cereus G9241), но у него обнаружена плазмида, pBCXО1, чья нуклеотидная последовательность на 99,6 % оказалась идентичной кодирующей токсин плазмиде pXO1 В. anthracis И хотя другая плазмида сибиреязвенного микроба, рХО2, кодирующая гены капсулы, обнаружена не была, генный кластер, кодирующий так) ю же капсулу, был обнаружен в ранее неизвестной плазмиде цереуса, названной рВС218. Эволюционное древо, показывающее место В. anthracis среди близкородственных бацилл, приведено на рис. 3.3.
Читать дальше









![Михаил Супотницкий - Очерки истории чумы. Книга II. Чума бактериологического периода [без иллюстраций]](/books/416279/mihail-supotnickij-ocherki-istorii-chumy-kniga-ii-thumb.webp)
![Михаил Супотницкий - Очерки истории чумы. Книга I. Чума добактериологического периода [без иллюстраций]](/books/416280/mihail-supotnickij-ocherki-istorii-chumy-kniga-i-ch-thumb.webp)

