Flaviviridae, экологически относящийся к арбовирусам, переносимым членистоногими. Семейство вирусов
Flaviviridae теперь выделено из семейства
Togaviridae и состоит из трех родов: флавивирусов
(Flavivirus), пестивирусов
(Pestivirus) и вирусов гепатита С и G
(Hepacivirus). Эти три группы вирусов, хотя имеют различные биологические свойства и не обладают серологической перекрестной реактивностью, похожи и родственны между собой, с точки зрения морфологии вирионов, организации вирусного генома и предполагаемой стратегии репликации геномной РНК. Все три рода семейства флавивирусов одинаково характеризуются инфекционной геномной РНК, сходной локализацией генов структурных белков на 5’–конце РНК, отсутствием специализированных геномных РНК, кодирующих белки вирионов, и образованием единого полипротеина–предшественника.
ВКЭ, как и вирионы всех флавивирусов, имеет сферическую форму диаметром до 50–60 нм, покрытую гликопротеиновой оболочкой. Внутри внешней оболочки размещается вирусный капсид – геномный нуклеопротеиновый комплекс, покрытый Core–белком, диаметром около 30 нм.
Геном флавивирусов в составе нуклеокапсида представлен одной молекулой однонитчатой РНК положительной полярности общей длиной около 11 тыс. нуклеотидов, которые кодируют полипептидную цепь длиной 3,4–3,6 тыс. аминокислотных остатков (а.о.). Вирусная РНК содержит 7–метилгуанозиновый кэп на 5’–конце. Геномная РНК служит в качестве мРНК для внутриклеточного синтеза вирусных белков. Для сборки зрелого флавивируса синтезируются 3 вирусных структурных белка: капсидный белок С, мембранный белок М и поверхностный белок Е. Незрелые внутриклеточные вирусные частицы содержат гликозилированный белок–предшественник ргеМ. Кроме того, в геноме флавивирусов закодированы неструктурные белки NS 1–NS 5, вирусная РНК–полимераза, которые обнаружены в инфицированной клетке и участвуют в репликации вируса. В геноме все белки закодированы последовательно в виде одной открытой рамки считывания. Индивидуальные белки вируса образуются в результате ко– или посттрансляционного расщепления единого вирусного полипротеина–предшественника протеазами вирусного или клеточного происхождения.
В репликативном цикле геномная РНК является инициатором инфекционного процесса и служит матрицей для создания дочерних копий.
Нуклеотидная последовательность всего генома ВКЭ и полная аминокислотная последовательность полипротеина вируса расшифрованы Плетневым с соавторами. На рис. 1 представлена линейная генетическая карта вируса с указанием кодируемых генов всех структурных и неструктурных белков и концевых нетранслируемых областей генома ВКЭ штамма Софьин.
Немного позже были расшифрованы полная нуклеотидная последовательность генома ВКЭ западного штамма Neudoerfi (Найдорф), дальневосточного штамма 205 и другого вируса из антигенного комплекса ВКЭ – вируса Повассан.
Первым с N–концевой части полипротеина ВКЭ находится нуклеокапсидный Core–белок С. Молекулярная масса – 12108 Da. При сборке вируса он вместе с геномной РНК образуют центральную структурную компоненту нуклеокапсида.
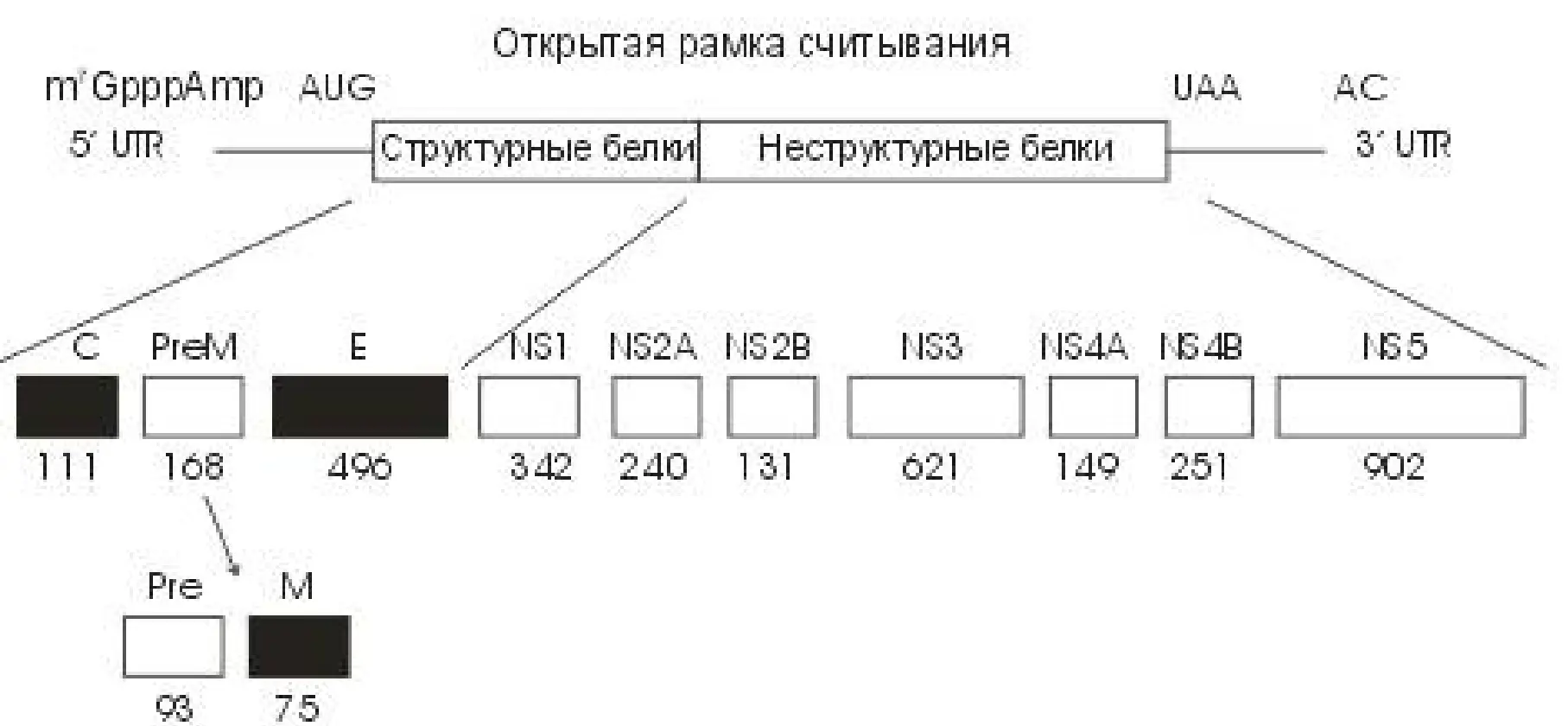
Рис. 1. Структура генома ВКЭ. Расположение концевых нетранслируемых областей, С, PreM (Pre+M), E и NS1–NS5 генов соответствующих структурных и неструктурных белков вируса.
Следующим от N–конца фрагментом полипротеина, отщепляемым протеазами, является гликопротеин ргеМ–полипептид. PreM является только предшественником в синтезе вирионного белка М, его нет в составе зрелого вириона в крови, не удается обнаружить его и в зараженных вирусом клетках. Мембранный белок М, содержащийся в составе оболочки зрелого вируса, представлен 75 остатками аминокислот, имеет молекулярную массу 8209 Da.
Следующим, отщепляемым от предшественника полипептидом является наиболее важный поверхностный вирионный белок Е – главный, биологически наиболее значимый компонент внешней поверхности оболочки вириона. Он играет ключевую роль в процессах сборки вирусной частицы, в связывании вируса с клеточной поверхностью, последующем слиянии вирусной и клеточной мембран, развитии гуморального и клеточного иммунитета. Полипептидная цепь белка Е с молекулярной массой 53680 Da, заканчивается двумя гидрофобными участками, вероятно, служащими трансмембранным «якорем» белка. Считается, что процессинг полипротеина между белком Е и неструктурным белком NS1 осуществляет связанная с мембранами аппарата Гольджи протеиназа.
Читать дальше













