Среди PRRs центральное место занимают Toll- like рецепторы (TLR), которые управляют целым рядом эффекторных функций (хемотаксис, фагоцитоз, респираторный взрыв, дегрануляция нейтрофилов, синтез эффекторных и регуляторных молекул), а также активируют и регулируют адаптивный иммунный ответ (адаптивная/ приобретенная иммунная система), необходимый (-ая) для узнавания более сложных высокоорганизованных изменяющихся молекулярных структур (белков). В процессе формирования и реализации функций клеток врожденной иммунной системы (дендритные клетки, макрофаги, нейтрофилы, тучные клетки, эозинофилы и др.), происходит изменение их поверхностных структур, активация захвата АТ, и изменение эффекторных механизмов. И вследствие этого, происходит обеспечение контроля иммунного гомеостаза: полная реализация эффекторных реакций врождённой иммунной системы и индукция приобретённого иммунитета.
Среди PAMPs выделяют:
MAMPs (микробно- ассоциированные молекулярные паттерны), преимущественно- рецепторы флагеллина (липополисахариды, манноза, пептидогликаны, липопротеины). Установлена зависимость распознавания флагеллина от рецепторного гена FLS2. В результате взаимодействия флагеллина и продукта гена FLS2- трансмембранная рецептподобная протеинкиназа, происходит активация каскада митогенактивируемых протеинкиназ и как итог- индукция комплекса защитных реакций в виде иммунного распознавания;
DAMPs (ассоциированные с повреждением молекулярные паттерны) – молекулярные фрагменты, способные инициировать неинфекционный воспалительный ответ на неинфекционный возбудитель. При повреждении тканей генерируются следующие структуры DAMPs: S100 белок (участвует во внутриклеточной и внеклеточной регуляции: клеточный рост и дифференциация, транскрипция, прогрессия клеточного цикла, организация клеточных мембран и динамика цитоскелета, защита от оксидативного повреждения клетки, секреция, фософолирование). Его повышенная концентрация в крови может свидетельствовать о образовании и развитии в организме меланомы, активно продуцирующей S100 и массивная гибель нейронов и как последствие- высвобождение белка S100 в общий кровоток. Таким образом, ECLIA- электрохемилюминнсцентный анализ- позволяет диагностировать рак кожи и заболевания ЦНС (травмы ГМ, ОНМК, нейдегенерация, болезнь Крейтцфельда- Якоба и др.) Белки теплового шока (HSP): поддержание структуры стероидных рецепторов и факторов транскипции, принимает участие в сворачивании и разворачивании белков, тем самым, обеспечиваю клетке нечувствительность к нагреванию, а именно их транскрипционный фактор, регулирующий экспрессию гена Hsp70, который является фактором канцрогенеза. Помимо этого, ингибирование HSP позволяет бороться против некоторых видов рака.
TLRs, о которых мы говорили раньше, способны идентифицировать и связываться с обеими видами паттернов. Сами по себе TLRs представлены как трансмембранные интегральные белки и между своими представителями имеют сходное строение. Структура молекулы представлена из нескольких содержательных компонент: поверхностная зона- N-концевая область аминокислотной последовательности из 19—25 участков, обогащённых лейцином (функция заключается в связывании лиганда). Далее- переходный участок, отвечающий за прикрепление рецептора к клеточной мембране, содержащий в себе преимущественно цистеин. Внутренняя дистальная часть рецептора представлена TIR доменом, имеющий сходное строение с семейством цитокинов IL-1.
В зависимости от локализации TLRs в клетке выделяют рецепторы, расположенные на цитоплозматической мембране и на мембранах внутриклеточных органелл- лизосом, эндосом, аппарат Гольджи; лигандами самих рецепторов являются поверхностные структуры микроорганизмов- липопротеин, липополисахариды, флагеллин, зимозан.
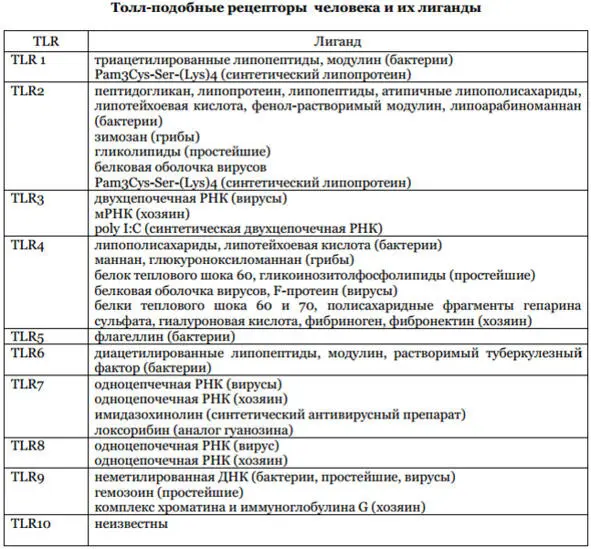
Ниже будут представлены все собранные сведения о TLR в виде проведенных исследований за 2016—2017 гг.
TLR-1- мембранный белок, распознающий патоген-связанные молекулярные структуры грам- положительных бактерий: пептидогликаны и липопептиды. Способен образовывать комплекс с TLR-2. Присутствует на всех лейкоцитах; обладает самой высокой экспрессией среди членов своей группы.
Чтобы проверить общие и редкие ТЛР варианты, участвующие в предрасположенности или резистентности к инфицированию микобактериями туберкулеза мы проанализировали экзоны генов, кодирующих ТЛР 1, 2, 4, и переходник молекулы TIRAP в более чем 4500 случаев туберкулеза (ТБ). Проведенный анализ позволил определить 109 вариантов с возможными функциональными воздействиями, в том числе 101 не синонимичный вариант. Анализ ассоциации дал значительный результат: 533 афроамериканца подтвердили защитный эффект и вызывает обмен аминокислоты из гистидина на лейцин в позиции 305.
Читать дальше
Конец ознакомительного отрывка
Купить книгу












