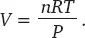Через какое-то время нефть закончится, так что, возможно, не так уж и плохо будет сдуть пыль со старых методов Вейцмана, тем более что производимый с их помощью в больших количествах бутанол теперь стал важным и ценным для химической промышленности продуктом.
Несчастливый корабль Артура Коундена HMS Shark находился под верховным командованием контр-адмирала Дэвида Битти, который видел, как через 20 минут после начала боя затонули два его линейных крейсера. Он резко заметил: «Кажется, с нашими чертовыми кораблями сегодня что-то не так». Некоторые утверждают, что корень проблемы был в кордите, поскольку его штабеля вызвали дальнейшие губительные взрывы после немецких ударов, которые корабли при обычных условиях должны были выдержать. Недавно морские археологи обследовали обломки одного из кораблей Битти, HMS Queen Mary («Королева Мэри») [191] Burr L. British Battlecruisers 1914–1918. Osprey Publishing, 2006.
, но все же трудно будет когда-либо прийти к определенному заключению по этому вопросу.

Рисунок 33.Профессор Хаим Вейцман (передний план): химик, пионер биотехнологий и политик-сионист с друзьями в верхах. © Институт Вайцмана.
Похоже, что на некоторых кораблях нарушались строгие правила обращения с шелковыми мешками, в которых хранился кордит, или что эти правила мешали орудиям стрелять с запрашиваемой скоростью. Что касается роли ацетона, то нам известно, что в оружейных запасах на HMS Queen Mary находилась как более старая версия кордита – cordite Mk.I , так и улучшенный cordite M.D ., в котором было гораздо меньше нитроглицерина [192] Brown D.K. The Grand Fleet: Warship Design and Development, 1906–1922 // Naval Institute Press, 2010 (1-е издание: Chatham, 1999).
. Неясно, было ли причиной то, что первая версия считалась безопасной, или то, что из-за нехватки ацетона было слишком дорого заменять его на версию M.D . Как бы то ни было, кажется, главной проблемой версии Mk.I был не повышенный риск взрыва, а скорее эрозия орудийных стволов.
Корабль HMS Shark не имел непосредственных проблем с кордитом, а затонул, «сражаясь до последнего», как сказано в Британской энциклопедии 1960 года издания. Его капитан Лофтус Джонс был посмертно награжден крестом Виктории. Шестерых выживших подобрал датский корабль, приставший к берегу в Халле, но самый юный (с большой вероятностью) член команды нигде не упомянут [193] Loftus Jones VC: A Biography. Royal Naval Museum Library, Portsmouth, 2005.
. В этом году 31 мая я снова сел в трамвай до кладбища Квиберг и положил цветы на могилу моей бабушки и на могилу бедного Артура Коундена.
И наконец, я хотел бы подхватить нить повествования из прошлой главы и спросить: так что же производит разрушительную силу взрыва? Ответ заключается в уравнении состояния идеального газа, с которым мы встречались в главе 3, и в реакции разложения – к примеру, нитроглицерина. Химики записали бы ее в виде вот такого уравнения, в котором (ж) обозначает жидкость, а (г) – газ:
4C 3H 5(NO 3) 3(ж) → 6N 2(г)+10H 2O (г)+12CO 2(г)+O 2(г).
Четыре молекулы жидкого нитроглицерина образуют 29 небольших молекул четырех видов газа. Объем этих молекул в газообразном состоянии можно рассчитать, применив уравнение состояния идеального газа, по формуле:
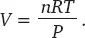
Вода тоже будет находиться в газообразном состоянии, поскольку во время реакции выделяется большое количество тепла – такая реакция называется экзотермической . (Имея некоторые дополнительные данные и воспользовавшись приведенной выше формулой, мы даже смогли бы точно подсчитать, сколько выделится тепла.) Если мы возьмем чайную ложку (5 мл) жидкого нитроглицерина, мы сможем подсчитать, сколько выделится молекул газа ( n ), так как при этом нам заранее известны давление ( Р ) и температура ( Т ) [194] Для тех, кому интересны подробности: мы используем уравнение состояния идеального газа в виде V = nRT/P с универсальной газовой постоянной R = 0, 082 л⋅атм/(моль⋅К), Т = 398 К, Р = 1 атм. С плотностью нитроглицерина в 1,6 г/см3 и молярной массой 227 г/моль мы получаем 8 г нитроглицерина, которые дают 0,035 моля. Общее количество молекул газа составляет 29×0,035/4 = 0,255 моля, а объем (V) = 0,255×0,082×398/1 = 8,3 л.
. Оказывается, эти 5 мл за доли секунды создадут более 8 литров горячего газа – это колоссальное увеличение в объеме, которое в буквальном смысле разнесет на кусочки все, что встретит на своем пути.
Читать дальше
Конец ознакомительного отрывка
Купить книгу