Это и в самом деле весьма странные молекулы, которые можно рассмотреть получше, если отойти от формального схематичного изображения, показанного на рисунке 27, и вместо этого попытаться представить себе размер молекулы и содержащихся в ней атомов. По мере того как мы добавляем протоны и нейтроны к атомным ядрам и продвигаемся от более легких элементов с низким зарядовым числом к более тяжелым, ядра, разумеется, увеличиваются в размере, но лишь в небольшой степени, так как большая часть пространства в атоме занята летающими электронами. С увеличением количества протонов растет и заряд ядра – соответственно, и сила, притягивающая к ядру электроны. Это означает, что атомы имеют склонность уменьшаться по мере увеличения зарядового числа. С другой стороны, должно расти и число электронов, и, когда эти отрицательно заряженные элементарные частицы приближаются к ядру, они начинают отталкивать друг друга, из-за чего атом кажется больше.
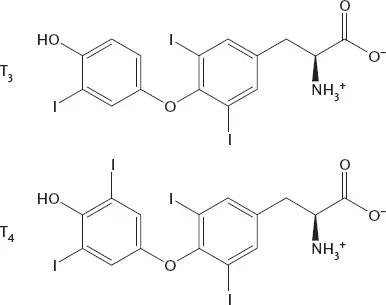
Рисунок 27.Гормоны щитовидной железы трийодтиронин и тироксин, известные также как Т 3и Т 4из-за количества атомов йода, прикрепленных к их органическому скелету. Изображенная жирной линией связь с группой NH 3 +означает, что эта связь выходит из плоскости и направлена в вашу сторону.
Которая из сил одержит верх? Это легко рассчитать, взглянув на Периодическую таблицу: если двигаться по периодам (строкам) слева направо, побеждает сила притяжения, и атомы становятся немного меньше; если двигаться по группам (столбцам) сверху вниз, побеждает сила отталкивания, поскольку после достижения конфигурации каждого из благородных газов (элементы в крайнем правом столбце) электроны добавляются на орбитали, или оболочки за пределами плотной внутренней электронной оболочки в атоме, соответствующей конфигурации благородного газа, и не особенно ощущают влияние дополнительного заряда ядра.
Химия не была бы химией, если бы не существовало исключений для этого правила; однако их мы рассмотрим в другой главе. Достаточно понять, что, спустившись по галогеновой лестнице от фтора (F) к хлору (Cl) и брому (Br), мы добираемся до атома йода, который совершенно не похож своими размерами на атом углерода. Взгляните на изображение, показанное на рисунке 28, и вы увидите, насколько сильно на нем преобладают атомы йода, которые на палочковой схеме совершенно идентичны остальным атомам.
Но дело не только в размере. Йодид-заместители (их так называют потому, что мы рассматриваем их как атомы, заменившие собой атом водорода в шестиугольном углеродном цикле С 6) на самом деле не обладают красивой округлой формой, а их электроны не движутся равномерно вокруг ядра; система больше напоминает фаршированные оливки, где связь углерод-йод вставлена прямо в красноватую начинку. Оливково-зеленая поверхность притянула избыточные электроны и имеет отрицательный заряд, а область начинки лишилась электронов, и там проглядывает положительно заряженное ядро, придавая этой части положительный заряд.
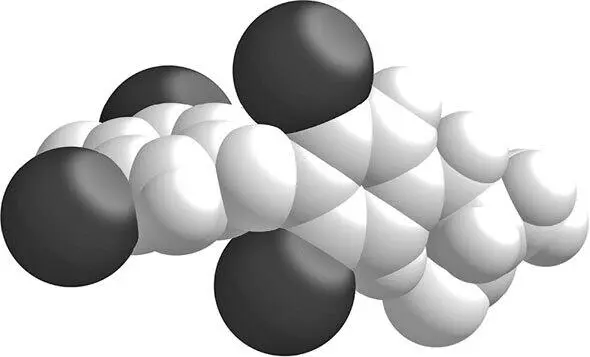
Рисунок 28.Здесь мы попытались изобразить истинный размер атомов в Т 4 – гормоне щитовидной железы тироксине, – нарисовав их в виде сфер разного размера. Обратите внимание на то, как доминируют на этом изображении крупные темные атомы йода, хотя они составляют менее 9 % от общего числа атомов в этой молекуле (все остальные атомы показаны светло-серым цветом).
Это означает, что атом – обычно это атом кислорода, – в котором есть пара электронов, очень заметно торчащая наружу (так обычно и происходит в аминокислотах, образующих наши белки), может зацепить молекулы Т 3и Т 4, направив эту электронную палку на красную положительно заряженную начинку и образовав слабую химическую связь. Именно так гормоны щитовидной железы выполняют свою важную задачу в организме: они передают сигналы, которые не только регулируют рост, развитие нервной и половой системы, но также контролируют химические пути расщепления пищи, извлечения энергии и производства тепла.
Разумеется, правильно работающая щитовидная железа крайне важна для нашего здоровья, и существуют самые разные связанные с ней заболевания и симптомы. Однако давайте на некоторое время остановимся на том, что в начале ХХ века верно определили скорее как нехватку микроэлемента, нежели как болезнь, – на зобе и кретинизме.
Читать дальше
Конец ознакомительного отрывка
Купить книгу














