Некоторые «пустые клеточки» были заполнены еще при жизни Менделеева. Это принесло ему мировую славу, ибо всем стало ясно, что составление этой таблицы — не просто формальный акт, а открытие великого закона природы.
Смысл порядкового номера, который приписывает таблица химическому элементу, стал очевидным лишь после того, как у физиков не осталось сомнений в справедливости планетарной модели атома Резерфорда и законов квантования энергии. Каков же этот смысл? Ответ оказывается на редкость простым: порядковый номер равен числу электронов, вращающихся около ядра. Можно сказать и так: порядковый номер элемента — это положительный заряд его ядра, выраженный в единицах заряда электрона.
Периодический закон Менделеева, принцип квантования энергии и изучение характеристических оптических и рентгеновских спектров атомов (о них мы расскажем попозже) позволили попять причину тождественного химического поведения атомов, стоящих в одном столбце таблицы Менделеева.
Энергия атома есть энергия взаимодействия электронов с ядром. Поскольку энергия квантуется, то логично было бы допустить, что электроны каждого атома можно расположить в ряд по энергиям. Первый электрон связан с ядром наиболее сильно, второй слабее, третий еще слабее и т. д., так что электроны атома расположены по энергетическим ступенькам. Логика нас не подводит, но опыт приводит к уточнению этой картины. Во-первых, оказывается, что каждую энергетическую ступеньку может занимать не один, а два электрона. Правда, эти электроны не одинаковы, а отличаются друг от друга свойством, которое называется «спином». Свойство это векторное. Так что любители наглядности могут представить себе, что на заполненной ступеньке находятся две «точечки», снабженные стрелками, — одна стрелка смотрит «вниз», а другая «вверх».
Само слово «спин» возникло следующим образом. Это английское слово, которое в переводе на русский язык означает «быстро вращаться». Чтобы представить себе, чем отличаются два электрона, сидящие на одной ступеньке, предлагалось думать, что один электрон вращается по, а другой — против часовой стрелки около своей собственной оси. Эта модель была подсказана поверхностным сходством атома и планетной системы. Раз электрон — нечто вроде планеты, то почему-бы не разрешить ему вращаться около своей оси. Я должен очередной раз огорчить читателя: наглядно представить себе спин электрона — задача невозможная. А вот как его измерить, мы скажем в следующей главе.
Но это не единственное важное заключение (к которому нас привело внимательное изучение спектров атомов). Второе заключение состояло в том, что ступеньки энергии отстоят друг от друга на неравные расстояния и могут быть разбиты на группы.
За первой ступенькой, которую называют К -уровнем, следует энергетический разрыв и за ним группа из 8 электронов, обозначаемая буквой L , затем группа из 18 электронов, обозначаемая буквой М … Не будем описывать расположение уровней и порядок их заполнения для всех атомов. Картина оказывается не столь уж простой и описание ее потребовало бы много места. Детали в нашей маленькой книжке роли не играют, и про ступеньки я упомянул лишь для того, чтобы пояснить, в чем же сходство атомов, которые находятся друг под другом в таблице Менделеева. Оказывается, у них одинаковое число электронов на верхней группе ступенек.
Становится ясным химическое понятие валентности атома. Так, у лития, натрия, калия, рубидия, цезия и франция по одному электрону на верхней группе ступенек. У бериллия, магния, кальция и т. д. — по два электрона. Валентные электроны слабее всего связаны с атомом. Поэтому при ионизации атомов, стоящих в первом столбце, образуются легче всего однозарядные частицы. Ионы бериллия, магния и пр. несут на себе два заряда, и т. д.
ЭЛЕКТРИЧЕСКОЕ СТРОЕНИЕ МОЛЕКУЛ
Химики называют молекулой мельчайшего представителя вещества. Физики большей частью пользуются этим словом лишь в том случае, если этот мельчайший представитель реально существует как отдельное маленькое тело.
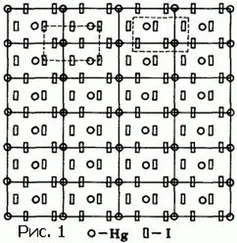
Существует ли молекула поваренной соли? Конечно, ответит химик, и напишет формулу: NaCl. Поваренная соль — это хлористый натрий. Молекула состоит из одного атома натрия и одного атома хлора. Однако этот ответ лишь формально справедлив. На самом же деле ни в кристаллике поваренной соли, ни в растворе соли в воде, ни в парах хлористого натрия мы не обнаруживаем пары атомов, которая вела бы себя как одно целое. Как мы говорили во второй книге, в кристаллике каждый атом натрия окружен шестью хлорными соседями. Все эти соседи равноправны, и никак нельзя сказать, какой из них «принадлежит» данному атому натрия.
Читать дальше