A + B =K + L.
Если новые молекулы прочнее старых (их суммарная энергия связи больше, чем у исходных молекул), то в результате реакции выделяется энергия. Действительно, на разрушение молекул Аи Вмы должны затратить меньше энергии, чем ее выделяется при образовании Ки L.Такие реакции называются экзотермическими, а количество выделяющейся энергии (на одну молекулу или на единицу массы вещества) носит название теплового эффекта. Например, тепловой эффект реакции горения бензина составляет сорок пять миллионов джоулей (около десяти тысяч килокалорий) на один килограмм. Этого тепла достаточно, чтобы нагреть продукты горения до температуры в несколько тысяч градусов.
Если реакция идет с выделением тепла, это не означает, что она пойдет быстро. Ведь прежне чем образовать новые связи, нужно разрушить старые. А для этого нужно где-то взять энергию. Так, туристская группа, маршрут которой проложен из одной долины в более глубокую, должна сначала подняться на перевал. Энергия, необходимая для разрыва или существенного ослабления (достаточного для протекания реакции) связей в исходных молекулах, называется энергией активации. На рис. 2 изображены энергетические барьеры для экзотермической ( а) реакции и реакции, идущей с поглощением тепла ( б- эндотермический процесс). Величина Е-энергия активации, или тот барьер, который должны преодолеть исходные молекулы, чтобы вступить в реакцию, Q- тепловой эффект реакции.
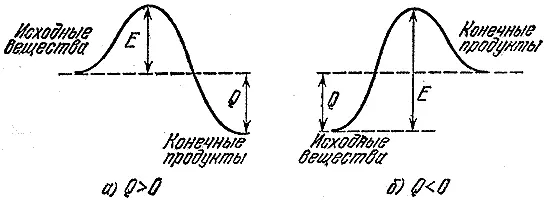
Рис. 2
Разрушение или ослабление химических связей может произойти под действием теплового (поступательного или колебательного) движения атомов и молекул. Природа устроена так, что энергия теплового движения при умеренных температурах обычно много меньше энергии активации. Так, для типичных реакций горения энергия активации в десятки тысяч раз превышает энергию теплового движения молекул. В этом причина столь малой скорости химического превращения при обычных температурах.
В газе при нормальных условиях каждая молекула испытывает в среднем десять миллиардов столкновений в секунду. Если бы каждое столкновение приводило к реакции, то она произошла бы мгновенно. Опыт не подтверждает этого. Например, смесь водорода и кислорода (гремучий газ) при комнатной температуре можно хранить совершенно спокойно. Все дело в том, что лишь очень малая доля столкновений оказывается эффективной, т.е. приводит к образованию воды. Большинство соударений оказываются бесполезными - химическая реакция идет лишь между теми молекулами, тепловая энергия которых намного превышает среднюю. А таких молекул очень мало. Из огромного числа молекул, содержащихся в кубическом сантиметре газа, лишь несколько имеют запас тепловой энергии, достаточный для того, чтобы пошла химическая реакция.
Однако доля активных молекул очень сильно возрастает с повышением температуры. Соответственно растет и скорость химической реакции. Чтобы почувствовать это, проще всего обратиться к числам. Реакция образования йодистого водорода из молекул водорода и йода при 290 К (комнатная температура) практически не идет: за миллион лет прореагировала бы всего одна тысячная процента смеси. Если же повысить температуру всего в два раза (до шестисот градусов Кельвина), то реакция в смеси закончилась вы всего за полтора часа. А при температуре в восемьсот градусов смесь прореагировала бы в течение секунды.
Для многих химических реакций справедливо следующее, довольно грубое, утверждение: повышение температуры на десять градусов приводит к удвоению скорости реакции.
Это свойство химических реакций природа использовала в процессе эволюции живых существ. Некоторые млекопитающие в трудное для них время года, зимние месяцы, впадают в спячку. При этом температура тела падает и лишь на несколько градусов превышает температуру окружающей среды. Жизненные процессы резко замедляются, что позволяет организму ограничить отдачу тепла наружу и преодолеть трудности, связанные с нехваткой питания. Наоборот, иногда выгодно повысить температуру тела (например, во время болезни) для того чтобы усилить обмен веществ и ускорить течение жизненных процессов. С этим успешно справляются органы терморегуляции организма.
Свойство химических реакций сильно ускоряться с повышением температуры лежит в основе объяснения и процессов горения.
Читать дальше
Конец ознакомительного отрывка
Купить книгу






![Майкл Муркок - История Рунного посоха [4 книги - Голова с камнем; Амулет Безумного Бога; Меч Рассвета; Рунный посох]](/books/391676/majkl-murkok-istoriya-runnogo-posoha-4-knigi-golo-thumb.webp)
![Майкл Азеррад - Come as you are - история Nirvana, рассказанная Куртом Кобейном и записанная Майклом Азеррадом [litres]](/books/392533/majkl-azerrad-come-as-you-are-istoriya-nirvana-ra-thumb.webp)



