Бесконечно разнообразны структуры кристаллов химических соединений. Крайними - в смысле различий - примерами могут служить структуры каменной соли и двуокиси углерода, изображенные на рис. 2.19 и 2.20.
Кристаллы каменной соли (рис. 2.19) состоят из чередующихся вдоль осей куба атомов натрия (маленькие темные шары) и хлора (большие светлые шары). Каждый атом натрия имеет шесть равноотстоящих соседей другого сорта. То же относится и к хлору. Но где же молекула хлористого натрия? Ее нет; в кристалле отсутствует не только группа из одного атома натрия и одного атома хлора, но и вообще какая бы то ни было группа атомов не выделяется своим сближением среди других.
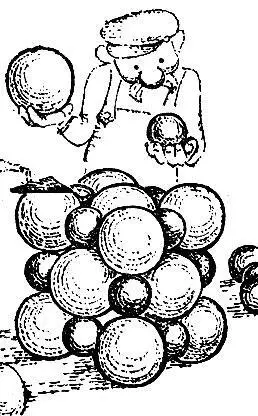
Рис. 2.19
Химическая формула NaCl не дает нам оснований говорить, что "вещество построено из молекул NaCl". Химическая формула указывает лишь, что вещество построено из одинакового числа атомов натрия и хлора.
Вопрос о существовании молекул у вещества решается структурой. Если в ней не выделяется группа близких атомов, то молекул нет.
Кристалл углекислого газа С0 2(сухого льда, который лежит в ящиках у продавщиц мороженого) - пример молекулярного кристалла (рис. 2.20). Центры атомов кислорода и углерода молекулы С0 2расположены вдоль прямой линии (см. рис. 2.2). Расстояние С-О равно 1,3 Å, а расстояние между атомами кислорода соседних молекул - около 3 Å. Ясно, что при таких условиях мы сразу же "узнаем" молекулу в кристалле.
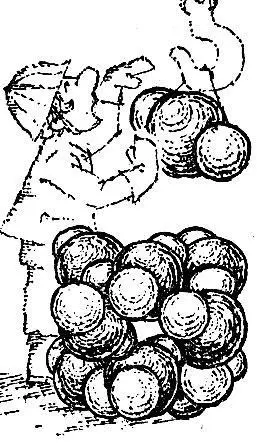
Рис. 2.20
Молекулярные кристаллы представляют собой плотные упаковки молекул. Чтобы это видеть, надо обрисовать контуры молекул. Это и сделано на рис. 2.20.
Все органические вещества дают молекулярные кристаллы. Органические молекулы зачастую содержат многие десятки и сотни атомов (а о таких, которые состоят из десятков тысяч атомов, мы поговорим особо в отдельной главе). Изобразить их упаковку графически невозможно. Поэтому вы можете увидеть в книгах рисунки, подобные рис. 2.21.
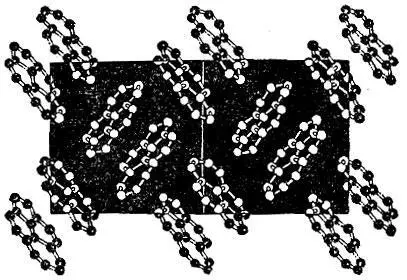
Рис. 2.21
Молекулы этого органического вещества составлены из атомов углерода. Стерженьки символизируют валентные связи. Молекулы как бы висят в воздухе. Но не верьте глазам своим. Чертеж сделан таким лишь для того, чтобы можно было рассмотреть, как расположены молекулы в кристалле. Для простоты авторы рисунка даже не изобразили атомов водорода, присоединенных к внешним атомам углерода (впрочем, химики так делают очень часто). Тем более авторы не сочли нужным "оконтурить" молекулу - придать ей форму. Если это сделать, то мы увидели бы, что принцип упаковки молекул - ключ к замку - работает в этом случае, как и в других ему подобных.
Поликристаллические вещества
Мы уже говорили о том, что аморфные тела - это редкость в мире твердых тел. Большинство окружающих нас предметов состоит из маленьких кристаллических зернышек, размерами около одной тысячной доли миллиметра.
Еще в прошлом веке зернистое строение металлов было обнаружено исследователями. Помог самый обычный микроскоп. Пришлось только приспособить его так, чтобы вести рассмотрение не "на просвет", а на отражение. Так поступают и сегодня.
Картинка, которая представляется глазу, показана на рис. 2.22. Границы зернышек обычно видны совершенно отчетливо. Как правило, на этих границах скапливаются примеси.

Рис. 2.22
От величины зерен, от того, что делается на их границах, от ориентации зерен зависят в огромной степени свойства материала. Поэтому физики потратили очень много труда на изучение поликристаллических веществ. То, что каждое зерно является кристалликом, было доказано с помощью рентгеноструктурного анализа, о котором мы уже обещали рассказать читателю.
Всякая обработка металла сказывается на его зернах. Вот получен кусок литого металла: зерна его расположены беспорядочно, размер их довольно велик. Из металла делают проволоку, протягивают ее. Как ведут себя при этом кристаллические зерна? Исследования показали, что изменение формы твердого тела при протягивании проволоки или при другой механической обработке вызывает раздробление кристаллических зерен. Одновременно под действием механических сил в их расположении появляется некоторый-порядок. О каком порядке может идти здесь речь? Ведь обломки зерен совершенно бесформенны.
Читать дальше