1.3 | Hydrologie im Zeitalter der Naturwissenschaften
Mit der Renaissance ab Mitte des 14. Jahrhunderts begann der Aufstieg der Naturwissenschaften allgemein und damit auch der Hydrologie. Die religiösen Dogmen der Kirche wurden durch Beobachtungen ersetzt, es entstand «Wissenschaft», wie man sie heute kennt. Wichtig für die Hydrologie sind zum einen die Schaffung der mathematisch-theoretischen Grundlagenund zum anderen der Aufbau von Messnetzenfür meteorologische Größen wie Temperatur oder Niederschlag und hydrologische Kennzahlen wie Wasserstand und Abfluss. Messungen begannen an einzelnen Orten um 1800, ab ca. 1900 gab es im deutschen Sprachraum verlässliche Messungen in größeren Netzwerken.
Viele Grundlagen der theoretischen Hydrologie wurden ebenfalls im ausgehenden 19. Jahrhundert gelegt. Henry Darcy (1803–1858) beschrieb den Zusammenhang zwischen Wasserhöhe, Durchlässigkeit und durchflossener Fläche in porösen Medien wie Böden. Der Abfluss im Gewässer war ebenfalls Gegenstand vieler Untersuchungen. Jakob Bernoulli veröffentlichte 1738 seine Untersuchungen zum Zusammenhang zwischen Geschwindigkeit und Druck. Der Mathematiker Leonhard Euler stellte die allgemeinen Bewegungsgleichungen für ideale Flüssigkeiten auf. Die erste empirische Gleichung zur Berechnung der Verdunstung als Funktion von Windgeschwindigkeit und Sättigungsdefizit geht auf John Dalton (1766–1844, publiziert 1801) zurück. Die quantitative Beziehung zwischen Niederschlag und Abfluss wurde bereits von Claude Perrault und Edme Mariotte im 17. Jahrhundert untersucht, aber erst 1932 stellte Leroy K. Sherman mit dem Einheitsganglinienverfahren eine empirische Beziehung zwischen den beiden Zeitreihen her.
1.4 | Wasserwirtschaft
Unabhängig vom theoretischen Verständnis des Wasserkreislaufs haben viele Hochkulturen Methoden zur Steuerung des Wasserhaushalts entwickelt. Zwei Bereiche der Wasserwirtschaft sind dabei oft verbunden mit Aufstieg und Niedergang von Hochkulturen: Bewässerung und Hochwasserschutz.Bewässerung schuf in vielen Kulturen die Voraussetzung für höhere landwirtschaftliche Erträge und ermöglichte deshalb die Entwicklung von Städten. Hochwasserschutz war oft verbunden mit technischen Hochleistungen wie Deichbau und erforderte eine hoch entwickelte Verwaltung zur Koordination der komplexen Baumaßnahmen. Auch der Bereich der Wasserver- und -entsorgung ist hier zu erwähnen: Die von den Römern gebauten Aquädukteund die Abwasserleitungen sind heute noch zu sehen (Abb. 1-2).
Vor allem in ariden Regionen sind der Aufstieg und der Niedergang von Kulturen oft direkt mit der Produktivität der Landwirtschaft, und damit mit der Bewässerung (→ Kap. 22) verbunden. Typische Beispiele dafür sind Mesopotamien im heutigen Irak und Iran sowie der Jemen. In Mesopotamien wurde Wasser in unterirdischen Kanälen, den sogenannten Qanaten, über viele Kilometer aus den Bergen in die Wüstenregionen transportiert.
Abb. 1-2 | Der Pont du Gard in Südfrankreich, ein von den Römern erbautes Aquädukt (Foto: Wikicommons).

Ein Beispiel der Verknüpfung von Wasserbau und nationalem Wohlstand ist der Ma‘rib-Dammim Jemen, dessen Überreste heute noch zu besichtigen sind. Mit dem Bau des Erddamms wurde ca. 1700 v. Chr. begonnen. Zur Zeit der Königin von Saba wurden mit dem Wasser des 14 m hohen Damms 100 km 2bewässert. Der erste größere Bruch des Damms ca. 145 n. Chr. führte zu einer verheerenden Flut. In der Folge wurde der Damm immer wieder repariert. Der endgültige Zusammenbruch erfolgte um 500 n. Chr. und führte zum Niedergang der Bewässerungslandwirtschaft und damit des ganzen Reichs.
Weiterführende Literatur
Biswas, A. K. (1970): History of Hydrology. Amsterdam/New York.
Deutsche Wasserhistorische Gesellschaft. URL: http://www.dwhg-ev.com/(Stand: 29.06.2015).
Garbrecht, G. (1996): Geschichte der Hydrologie. In: Baumgartner, A. und H.-J. Liebscher (Hrsg.): Lehrbuch der Hydrologie. 1. Band. Allgemeine Hydrologie. Quantitative Hydrologie. Stuttgart, S. 11–70.
| 2Wasser als Stoff
Martin Jekel, Andreas Grohmann
Inhalt
2.1 Molekularer Aufbau
2.2 Wasser als polares Molekül – Wasserstoffbrückenbindungen
2.3 Physikalische Eigenschaften
Wasser besitzt einzigartige Eigenschaften und ist für alle biologischen und ökologischen Vorgänge unverzichtbar. Sein molekularer Aufbau mit gewinkelten Bindungen zwischen Sauerstoff- und Wasserstoffatomen ist von zentraler Bedeutung für die Ausbildung von Wasserstoffbrückenbindungen. Alle physikalischen und chemischen Prozesse mit Wassermolekülen beruhen darauf und sind ungewöhnlich im Vergleich mit ähnlichen Molekülen.
2.1 | Molekularer Aufbau
Wasser(H 2O) ist die bei Weitem wichtigste binäre, aus Atomen zweier Elemente bestehende Verbindung. Sie entsteht aus der Vereinigung der Elemente Wasserstoffmit dem Elementsymbol H (gr.-lat. hydrogenium, «Wasserbildner») und Sauerstoffmit dem Elementsymbol O (gr.-lat. oxygenium, «Säurebildner»). Der Grundzustand der Elemente ist jeweils das zweiatomige Molekül H 2bzw. O 2. Namen im Rahmen der wissenschaftlichen Nomenklatur sind Dihydrogenoxidund Oxidan.
Wasser besitzt einzigartige physikalische und chemische Eigenschaften und ist für alle biologischen und ökologischen Vorgänge unverzichtbar. Diese Eigenschaften bedingen seine Rolle als Träger des Lebens und machen Wasser zum Ausgangspunkt einer Vielzahl von Wechselbeziehungen, die unseren blauen Planeten prägen. Die besonderen Eigenschaften des Wassers gründen in der Struktur des Wassermoleküls und in der Art der in ihm zwischen Sauerstoff- und Wasserstoffatomen geknüpften kovalenten Bindungen.
Das Element Wasserstoff findet sich in der 1. Hauptgruppe des Periodensystems bzw. der 1. Gruppe und der 1. Periode mit der Ordnungszahl 1, das Element Sauerstoff in der 6. Hauptgruppe, bzw. der 16. Gruppe und der 2. Periode mit der Ordnungszahl 8. Ein Wasserstoffatom mit dem Symbol H weist ein Elektron in seiner Elektronenhülle auf und ein Sauerstoffatom O acht Elektronen, davon sind sechs an Bindungen beteiligt. Die Elektronenkonfigurationdes Wasserstoffatoms im Grundzustand wird als 1s 1notiert, diejenige des Sauerstoffatoms als 1s 22s 22p 4. Die führenden Ziffern in dieser Notation sind die Hauptquantenzahlen der Elektronenhülle, die Kleinbuchstaben sind aus der Spektroskopie abgeleitete Bezeichnungen der besetzten Atomorbitale, und die Exponenten geben die Elektronenanzahl in den jeweiligen Atomorbitalen an. Die in diesen Orbitalen befindlichen Elektronen werden als Valenzelektronenbezeichnet.
Abb. 2-1 | Zwei Darstellungen der räumlichen Anordnung der Atome und freien Elektronenpaare im H 2O- Molekül. Der angegebene Bindungswinkel ist der für die Gasphase bestimmte Wert (nach Grohmann et al. 2011).
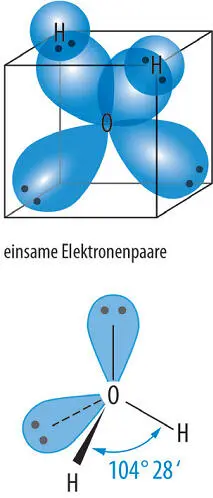
Das Wassermolekül hat die Form eines Tetraeders.
Die Verknüpfung von Atomen zu Verbindungen, wie z.B. die Bildung von Wasser (H 2O) aus einem Atom Sauerstoff und zwei Atomen Wasserstoff, befriedigt in der Regel das Bestreben der Atome, besonders stabile Elektronenkonfigurationenzu erlangen. Aus diesen Betrachtungen ergibt sich, warum die Summenformelfür das Wassermolekül H 2O lautet, sich also bei der Bildung von Wasser aus den Elementen genau zwei Wasserstoffatome mit einem Sauerstoffatom unter Ausbildung zweier kovalenter Bindungen verknüpfen. Im Zuge der Reaktion steuern zwei Wasserstoffatome je ein Valenzelektron und das Sauerstoffatom sechs Valenzelektronen bei.
Читать дальше


