Молекула водорода – это как два мячика, соединенные пружинкой, она может буквально вибрировать и вращаться, что открывает совершенно новый канал для потери тепловой энергии. Сталкивающиеся молекулы конвертируют часть энергии движения в энергию высвобождаемых фотонов. Эти довольно податливые молекулярные пружинки могут успокаиваться быстрее, чем атомы, которые ведут себя как твердые бильярдные шары, поэтому они быстрее остывают.
А значит, стоило Вселенной начать создавать из атомов водорода подобные простые молекулы, температура газа стала падать гораздо быстрее. Холодный газ хуже сопротивляется гравитационному сжатию, поэтому появление молекулярного водорода прямо привело к формированию первого поколения звезд. А в результате запустило и производство всех более тяжелых элементов.
Однако Н 2– не единственный сорт молекул водорода, который производит Вселенная. Если мы выясним, какие виды молекул встречаются в космосе, мы обнаружим, что второе место по численности после простой двухатомной версии молекул водорода занимает трехатомный вариант H 3. Это всего-навсего три протона, связанные двумя электронами, а поскольку третьего электрона молекуле не хватает, она в целом заряжена положительно.
Молекула H 3 ++весьма примечательна [148] См., например, обсуждении в статье B. J. McCall and T. Oka. H 3 + – an Ion with Many Talents // Science 287 (2000): 1941–42.
. Подобно обычной молекуле водорода, она играет важнейшую роль в остывании газа. Кроме того, она очень реактивна, и этим объясняется большинство так называемых молекулярно-ионных реакций в межзвездном пространстве. Ее спектроскопические среды мы обнаруживаем в самых удивительных местах, например, в атмосфере Юпитера. Вполне можно сказать, что обычная молекула водорода – это вселенская молекула-бабушка, а H 3– молекула-мать.
Если составить список химических реакций, в которых участвует H 3 ++, станет видно, что они очень разнообразны. В результате этих взаимодействий, в частности, получается вода. А еще – синильная кислота, которой у нас есть все основания остерегаться, однако следует помнить, что она же служит ингредиентом для создания различных предшественников биомолекул, в том числе аминокислот. Кроме того, в итоге цепочек реакций, которые запускает H 3 +, возникают метиловый и этиловый спирты и ацетилен [149] См. D. F. Strobel. Molecular Hydrogen in Titan’s Atmosphere: Implications of the Measured Tropospheric and Thermospheric Mole Fractions // Icarus 208 (2010): 878–86
. А когда мы проследим всевозможные варианты развития событий, то обнаружим, что именно H 3лежит у истоков формирования все более и более длинных цепочек молекул на основании углерода – структур, которые приближаются к биологическим молекулам так близко, что становится даже страшно.
Запуск химических реакций позволяет нам сделать далеко идущие выводы по поводу истоков космической химии. Как я уже упоминал, углерод – это атом, сочетание внешних электронов и общих размеров которого позволяет ему создавать поразительно разнообразные молекулярные структуры. А в сотрудничестве с H 3 ++он, судя по всему, способен на все в пределах термодинамических ограничений, которые налагает холод межзвездного пространства.
И в самом деле, астрономы и астрохимики обнаружили, что Вселенная прямо-таки полна углеродосодержащих молекул. При помощи разных астрономических приемов удалось выявить в космическом пространстве свыше 180 разных видов молекул, и более 70 % из них углеродосодержащие. Ожидается, что этот список – всего лишь верхушка айсберга, поскольку в космосе наверняка есть самые разные более крупные молекулы, однако, чем они больше и сложнее, тем труднее их зарегистрировать, поскольку их спектральные признаки сильно смазаны.
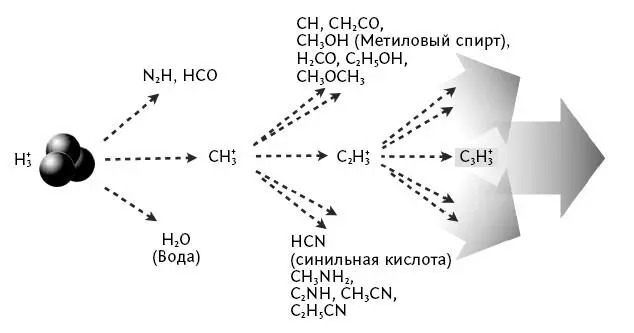
Рис. 12. Схема образования некоторых химических соединений с участием молекулы H 3 +.
Возможны также реакции, которые приводят к созданию все более и более длинных цепочек атомов углерода и возникновению самых разных молекул (справа).
Еще богаче ассортимент химических соединений в более плотной и бурной среде вокруг формирующихся звезд и планетных систем. Зачастую в таких местах наблюдается огромное количество молекул воды, а также самые разнообразные органические углеродосодержащие соединения, чем дальше, тем больше. Мы видим там молекулы спирта и сахара, а также следы предшественников аминокислот вроде глицина. Все это обретает особый смысл, если взглянуть на происходящее, вооружившись познаниями в химии. Одновременно с наблюдениями ученые разрабатывают и математические модели химических процессов, которые должны происходить в подобных средах, – и мы обнаруживаем, что на практике происходят именно такие реакции, возникают именно такие соединения, какие предсказываются моделями. Фундаментальная химическая теория предсказывает все, что мы видим, – но не только.
Читать дальше
Конец ознакомительного отрывка
Купить книгу










