Зола (обозначается буквой «А») – это минеральная часть топлива, включающая оксиды кремния, железа, алюминия, а также соли щелочных и щелочноземельных металлов.
Влага топлива (W) подразделяется на внешнюю и гигроскопическую. При длительном хранении твердого топлива в сухом месте оно теряет внешнюю влагу и становится «воздушно-сухим».
Таким образом, если какое-то количество топлива принять за 100 %, то можно записать:
C r+ H r+ O r+ N r+ S л r+ A r+ W r= 100 %. (2.1)
Индекс «r» в этом уравнении обозначает, что речь идет о рабочей массе топлива, полученного на электростанции (за рубежом обычно говорят не «рабочее», a «as receive», то есть «полученное» топливо).
Исключая из рабочего состава всю влагу, можно получить:
C d+ H d+ O d+ N d+ S л d+ A d= 100 %. (2.2)
Индекс «d» в этом уравнении обозначает «dry», то есть «на сухую массу».
Если пойти еще дальше и исключить золу (точнее – минеральную массу), то можно получить состав горючей массы топлива:
C daf+ H daf+ N daf+ O daf+ S л daf= 100 %. (2.3)
Индекс «daf» в этом уравнении обозначает топливо – «dry ash free», то есть «сухое и свободное от золы».
Сера со значком «л», входящая в вышеприведенные уравнения, во-первых, не включает серу, входящую в состав золы, и, во-вторых, состоит из двух частей: серы органической и серы колчеданной (Fe 2S), которая присутствует в некоторых марках углей в заметном количестве.
Следовательно, можно рассматривать еще и органическую массу топлива, которая не содержит серы колчеданной:
C o+ H o+ O o+ N o+ S o= 100 %. (2.4)
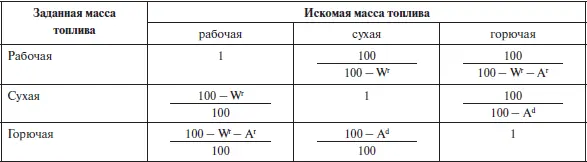
Для пересчета состава топлива, величины выхода летучих и теплоты сгорания с одной массы топлива на другую необходимо воспользоваться коэффициентами пересчета, приведенными в табл. 2.1.
Некоторые особенности при пересчете характеристик топлива возникают при использовании сланцев, имеющих повышенное содержание карбонатов. Если для обычных видов топлива горючая масса – это разница 100 – W r– А r, то при содержании карбонатов больше 2 % необходимо считать горючую массу по другой формуле:
100−W r−A испр r−(СО 2) K,
где А испр– зольность без учета сульфатов, образовавшихся при разложении карбонатов и с поправкой на сгорание серы колчеданной, то есть
A испр r= A r−[2,5(S a−S ст)d + 0,375 S к d]·(1−W r/100),
где S, S сти S к– содержание серы в лабораторной золе, сульфатной серы в топливе и колчеданной серы соответственно.
Горючими элементами топлива, как уже отмечалось, являются углерод, водород и сера. При полном сгорании с теоретически необходимым количеством окислителя эти компоненты выделяют разное количество теплоты:
С + О 2= CO 2− 8130 ккал/кг (34,04 МДж/кг);
2Н 2+ O 2= 2Н 2O − 29 100 ккал/кг (121,8 МДж/кг);
S + O 2= SO 2− 2600 ккал/кг (10,88 МДж/кг).
Следует учитывать, что углерод составляет большую часть рабочей массы топлива: в твердом топливе его доля равна 50–75 % (в зависимости от возраста углей), а в мазутах – 83–85 %. Водорода в топливе меньше, но он отличается очень высокой теплотой сгорания. Если продукты его сгорания сконденсировать (то есть учитывать не низшую, а высшую теплоту сгорания), выделенная теплота составит даже не 121,8, а 144,4 МДж/кг.
Серу отличает невысокая теплота сгорания, да и количество её, как правило, невелико. Следовательно, сера не представляет существенной ценности как горючий элемент, а вот проблемы, связанные с наличием SO 2в продуктах сгорания, – весьма существенны.
Таблица 2.1 Коэффициенты пересчета характеристик топлива
Всё вышесказанное относится в основном к твердому и жидкому топливам. Газ, в отличие от них, – механическая смесь нескольких компонентов. В природном газе большинства месторождений основной составляющей является метан – СН 4, количество которого колеблется от 85 до 96 %. Кроме метана, в составе природного газа обычно имеются более тяжелые углеводороды: этан С 2Н 6, пропан С 3Н 8, бутан С 4Н 10и др. Газ некоторых месторождений, кроме углеводородов, содержит и другие горючие компоненты: водород Н 2и оксид углерода СО. Из негорючих компонентов в состав газа входят азот N 2и диоксид углерода CO 2.
Основной характеристикой любого вида органического топлива является его теплота сгорания, то есть количество теплоты, выделяющейся при полном сгорании единицы массы (для твердого и жидкого топлива) или единицы объема (для газа). В расчетах чаще всего используют низшую теплоту сгорания (Q i r) – количество теплоты, образовавшейся при сжигании 1 кг угля или мазута, а при сжигании газообразного топлива – 1 м 3этого газа. При этом предполагается, что продукты сжигания остались в газообразном состоянии. Иногда используют другую теплотехническую характеристику – высшую теплоту сгорания (Q s r), но при этом в тексте обязательно уточняют, что речь идет именно о Q s r(или HHV – higher heating value, в отличие от LНV – lower heating value — низшей теплоты сгорания). Высшая теплота сгорания всегда больше, чем низшая, так как она учитывает дополнительное количество теплоты, выделяющейся при конденсации водяных паров и охлаждении всех продуктов сгорания до исходной температуры.
Читать дальше













