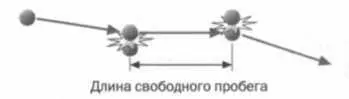
РИС . 2
Лошмидт оказался первым ученым, использовавшим понятие длины свободного пробега для вычисления числа и диаметра молекул газа, связав введенную Клаузиусом величину с пропорцией между объемом в газообразном состоянии вещества и объемом этого вещества в сжиженном состоянии. На основе этой идеи он смог установить, что в случае с воздухом один кубический метр содержит примерно 19 квадриллионов молекул, то есть 19 с 24 нулями. Вычисление Лошмидта стало первой оценкой постоянной Авогадро, устанавливающей число молекул в одном моле вещества (моль — химическая единица, макроскопическое представление атомной массы молекулы).
ЧИСЛО АВОГАДРО
Одна из самых важных величин в химии — это число Авогадро, которое, несмотря на название, было вычислено Лошмидтом. Оно обозначается так в память об Амедео Авогадро (1776-1856), впервые предположившем, что объем газа должен быть пропорционален числу содержащихся в нем молекул. Химикам привычно измерять вещества единицей под названием моль. Идея, лежащая в основе понятия моль, заключена в том, что число частиц важнее массы или объема. Так, один моль любого вещества (чистого или составного элемента) имеет ровно то же самое число частиц, что и моль другого вещества, в котором эти частицы могут быть атомами или молекулами. Другая важная величина — это атомная масса. Она определяется как отношение между средней массой атомов некоего элемента и 12-й частью массы углерода-12. Моль вещества определяется как атомная масса в граммах: например, один моль газа водорода (атомная масса 1), молекулы которого состоят из двух атомов, весит два грамма; один моль кислорода (атомная масса 16), молекулы которого также состоят из двух атомов, весит 32 грамма. Так остается постоянной пропорция между массами различных веществ. Следует подчеркнуть, что можно использовать понятие моля без детализации знаний о ядре атомов: нужно только иметь представление о пропорции между количеством веществ, вступающих в реакцию. Если мы знаем, что один моль кислорода весит 32 грамма, и замечаем, что он всегда реагирует с четырьмя граммами водорода, то. имея формулу Н 20, мы можем сделать вывод, что один моль водорода весит два грамма. Несмотря на то что Лошмидт вычислил плотность молекул на кубический метр воздуха, легко применить полученное им число для выяснения числа молекул в одном моле. Это 6,022 · 10 23, и оно известно как постоянная Авогадро.
Теперь мы уже можем понять содержимое статьи Больцмана 1866 года. Работа начиналась с определения температуры газа со средней кинетической энергией молекул. Для этого физик доказал, что в состоянии равновесия (в котором нет теплопередачи между одним веществом и другим, поскольку оба находятся при одинаковой температуре) также нет передачи кинетической энергии между молекулами этого вещества.
Но когда два вещества пребывают в неравновесии, кинетическая энергия молекул стремится переходить от более теплого к более холодному. То есть среднее значение кинетической энергии ведет себя точно так же, как и температура: отождествить их обе кажется самым естественным выводом.
Больцман прибегнул к любопытной гипотезе: он предположил, что движение молекул периодично. То есть при достаточном времени молекула будет менять значения энергии, пока не вернется к значению, которое имелось вначале. Также он добавил: "Если орбиты не замкнутся за конечное время, можно предположить, что это произойдет за бесконечное время". Идею можно интуитивно понять как то, что любая ситуация в итоге повторится, если подождать достаточно времени.
С толкованием температуры в терминах механики первое начало термодинамики было прояснено: как тепло, так и работа взаимозаменяемы, поскольку это просто формы движения. В первом случае — микроскопическое, во втором — макроскопическое. Оставалось обосновать второе начало, а это было намного сложнее, притом что энтропию столь сложно понять интуитивно. Для этого Больцман использовал сугубо математические аргументы, без углубления в физику, что было характерно для его более поздних работ. Ученый ограничился тем, что показал: тепло, понимаемое как поставляемая энергия, разделенное на температуру, полученную его выделением, порождает величину, которая ведет себя в точности как энтропия. В итоге он воспользовался макроскопическими термодинамическими аргументами (не интересуясь молекулярным поведением) для доказательства второго начала.
Читать дальше











