Главным противником Дальтона был Клод Луи Бертолле (1748-1822), для которого новые выкладки и теории о газовых смесях были не больше чем "игрой воображения". Как мы увидим в следующей главе, французский ученый в соответствии с идеями Ньютона разработал теорию химического сродства. Также он был наставником и учителем Луи-Жозефа Гей-Люссака. Несомненно, заслугой Бертолле является определение главного слабого места атомной теории, так что несправедливо говорить о нем как о противнике Дальтона. Более того, когда Дальтон приехал во Францию, чтобы познакомиться с главными учеными страны — Бертолле и Гей-Люссаком, его приняли со всеми почестями.
Труд "Новая система химической философии" был опубликован в двух томах, первый состоял из двух частей. Первая часть первого тома появилась в 1808 году. Джон Дальтон посвятил работу профессорам и сотрудникам шотландских университетов Эдинбурга и Глазго, которые всегда оказывали ему теплый прием и вдохновляли его в научных изысканиях. В посвящении также упоминались члены Lit & Phil, поддерживавшие исследования Дальтона.
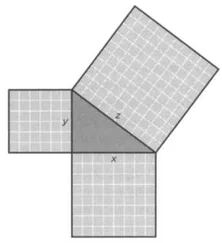
Первая часть, в свою очередь, делится на три главы. Первая посвящена теплу, вторая — строению тел, третья — химическому синтезу. Текст сопровождают четыре таблицы в конце книги. Самой известной является четвертая таблица, в которой Джон Дальтон привел произвольные обозначения выделенных им элементов. На первом месте 20 простых элементов, и здесь допущена лишь одна ошибка: окись кальция (известь, или негашеная известь, по-английски lime), формула которой — СаО. Она занимает восьмое место, и ее атомная масса равна 24.

Четвертая таблица, опубликованная впервой части первого тома "Новой системы химической философии" Дальтона, в которой он указывает атомную массу и произвольные обозначения выделенных им элементов.
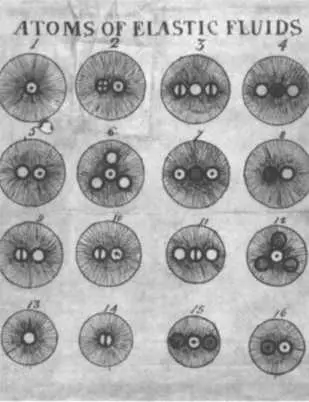
Седьмая таблица второй части первого тома, на которой изображен вид в профиль соединений упругих флюидов.

Бронзовая статуя Дальтона на улице Честер в Манчестере.
| номер |
элемент |
масса |
номер |
элемент |
масса |
| 1 |
водород |
1 |
11 |
стронций |
46 |
| 2 |
азот |
5 |
12 |
барий |
68 |
| 3 |
углерод |
5, 4 |
13 |
железо |
38 |
| 4 |
кислород |
7 |
14 |
цинк |
56 |
| 5 |
фосфор |
9 |
15 |
медь |
56 |
| 6 |
сера |
13 |
16 |
свинец |
95 |
| 7 |
магний |
20 |
17 |
серебро |
100 |
| 8 |
известь |
24 |
18 |
платина |
100 |
| 9 |
натрий |
28 |
19 |
золото |
140 |
| 10 |
калий |
42 |
20 |
ртуть |
167 |
В той же таблице Дальтон выделил пять двойных соединений (номера 21-25): вода, аммиак, азотная кислота, этилен, окись углерода; четыре тройных соединения (номера 26-29): закись азота, азотная кислота и углеродный водород (метан); четыре четверных соединения (номера 30-33): кислородноазотная кислота, серная кислота, сероводород и спирт; одно пятерное соединение (азотистая кислота), одно шестерное (уксусная кислота) и два семерных (нитрат аммония и сахар).
Вторая часть первого тома увидела свет в ноябре 1810 года, она была посвящена сэру Гемфри Дэви (профессору химии Королевского института) и Уильяму Генри (в то время вице-президенту Lit & Phil). Дальтон добавил две новые главы: четвертая описывала простые вещества, а пятая — соединения двух элементов по правилу наибольшей простоты. В этой второй части тоже мало таблиц, в основном в ней даны подробные описания собственных опытов автора. В пятой таблице приведены те же обозначения, что и в предыдущей, четвертой, но она исправлена и дополнена. Опыты позволили Дальтону выделить 36 элементов и 24 соединения. Никель, олово, висмут, сурьма, мышьяк, кобальт, марганец, уран, вольфрам, титан, церий, alumina (алюминий?), silex (кремний?), иттрий, бериллий и цирконий собраны в первой группе. В шестой таблице, представляющей собой что-то вроде продолжения пятой, появляются обозначения 27 соединений. Седьмая таблица изображает вид частиц, составляющих упругие флюиды (газы), а также частицы азота и водорода с их тепловой атмосферой. Наконец, в восьмой таблице Дальтон представил атомы 16 упругих флюидов (газов).
Читать дальше