Претерпевают изменения и митохондрии: матрикс светлеет, часто объем их возрастает, количество крист уменьшается, содержание осмиофильных гранул повышается. Последнее обстоятельство имеет биохимическое подтверждение в увеличении количества внутримитохондриального кальция, что характерно как для регенерирующих, так и для опухолевых тканей. Относительно быстро истощается компенсаторный резерв окислительного фосфорилирования и становится невозможным его эффективное функционирование в связи с низким напряжением кислорода и по другим причинам. Митохондрии клеток быстро пролиферирующих тканей по сравнению с неделящимися более чувствительны к повреждению в различных неблагоприятных для клетки условиях.
Уменьшается степень связи клеток в ткани, о чем свидетельствует увеличение размеров межклеточных пространств, снижение числа и размеров щелевых мостиков и других структур межклеточных контактов. Сокращение межклеточных контактов совпадает с изложенными биофизическими данными. В далеко зашедших случаях хронической ускоренной пролиферации может происходить потеря контактного торможения деления клеток.
Важно обратить внимание на то, что в клетках, длительное время ускоренно размножающихся, уменьшается число специализированных выростов и выпячиваний плазматической мембраны, содержащих различные рецепторные комплексы на гормоны белковой природы, антигены, гормональные регуляторы и др. Этот признак является морфологическим отражением утраты клеткой многих поверхностных глюко- и протеоконъюгатов, падения чувствительности делящейся клетки к внешним регуляторным влияниям. Происходит относительная «регуляторная глухота», снижение чувствительности ко многим гормонам белковой природы, действующим на уровне внешней стороны плазматической мембраны.
Средняя картина морфологической перестройки клетки в связи с длительной интенсификацией деления характеризуется сокращением количества и объема мембранных структур, выполняющих специализированные функции в интересах целого организма, и одновременно усилением структур, непосредственно связанных с функцией деления. Клетка морфологически упрощается и становится более похожей на независимо существующий одноклеточный организм (рис. 5).
Все изложенное приближает изначально дифференцированную зрелую клетку к ее эволюционно более древним предкам. Сокращение общей площади мембран клетки сочетается с биохимическими и биофизическими данными о нарушении интегральных функций мембран и связанных с ними структур и первичных регуляторных процессов.
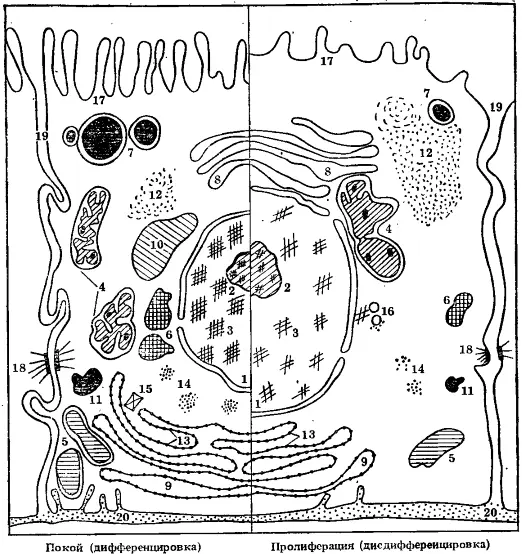
Рис. 5. Цитологическая перестройка «идеальной» животной клетки при переходе от состояния «покоя» (специфической функции в дифференцированном состоянии) к пролиферации (снижению специфической функции и дисдифференцировке)
1 — ядро; 2 — ядрышко; 3 — хроматин; 4 — митохондрии; 5 — лизосомы; 6 — микротельца; 7 — секреторные пузырьки; 8 — агранулярный эндоплазматический ретикулум; 9 — гранулярный эндоплазматический ретикулум; 10 — гранулы гликогена; 11 — капли липидов; 12 — свободные рибосомы; 13 — связанные рибосомы; 14 — полисомы; 15 — гранулы неорганических веществ; 16 — центриоль; 17 — микроворсинки; 18 — межклеточные контакты; 19 — межклеточные пространства; 20 — базальная мембрана
Способность к пролиферации — древнейшее свойство клеточного уровня организации биологических систем. Специфические функции клетки, возникшие в ходе дифференцировки у многоклеточных организмов, относятся к более поздним эволюционным приобретениям. Эти функции связаны с разделением обязанностей и специализацией отдельных клеток в интересах целого организма.
Переход клетки и ткани от выполнения специализированной функции в системе целостного организма, т. е. от дифференцированного состояния, к снижению дифференцировки и усилению пролиферации означает переход на эволюционно более древние и более устойчивые пути метаболизма. Обнаружение в активно или длительно пролиферирующих тканях каких-либо эмбриональных свойств (ферментов, антител и т. п.) следует рассматривать как проявление эволюционно-древних признаков.
Ошибки синтеза белка при усилении пролиферативной активности ткани
Читать дальше













