Ван Гельмонт в течение 5-ти лет выращивал иву [96], проводя точные замеры весовых характеристик дерева, почвы и поливальной воды. По завершению опыта ван Гельмонт обнаружил, что ива за 5 лет прибавила в весе на 74 кг (164 фунта), а земля, в которую ива была высажена, убавилась в весе лишь на 57 г. (2 унции). Это привело ван Гельмонта к выводу, что существуют всего два элемента – вода и воздух. А третий элемент – вещественный – включающий растения, деревья, и т.д., и даже землю, образуется в основном из воды. Не признавал ван Гельмонт и элемент «огонь», хотя вполне ясно, что ива, выращенная в темном помещении, будет существенно отличаться от ивы, выращенной ван Гельмонтом на солнечном свете. Пренебрег в своем опыте ван Гельмонт и газовым обменом растения, в данном случае ивы, что тем более удивительно, тем, что именно ван Гельмонт первым обозначил группу летучих химических веществ термином «газ», от греческого слова «χάος», а до ван Гельмонта применялся термин «αέρας» – воздух.
Химики с 1600 г. занимались многими вопросами в области научных химических опытов со многими веществами, но изучение воды, как основного элемента всей природы, целенаправленно проводили мало. Отметим основные достижения.
В 1665 г. голландский механик Христиан Гюйгенс (1629—1695) предлагает, как основные точки для термометра, точки плавления льда и кипения воды.
В 1667 г. Гюйгенс показывает, что вода при замерзании расширяется со значительной силой, в опыте он разрывает железную трубку силой замерзающей воды.
В 1674 г. французский физик Дени Папен (1674—1713) наблюдает зависимость температуры кипения воды от давления и устанавливает факт, что при более низком давлении вода закипает при более низкой температуре. Он же в 1681 г. проводит опыт на котле с предохранительным клапаном, и устанавливает повышение температуры закипания воды с увеличением давления в закрытом котле.
В 1704 г. английский физик Исаак Ньютон (1642—1727) изучал цвет чистой воды и определил его как зеленый.
В 1755 г. швейцарский ученый Жан Андре Делюк (1727—1817) впервые наблюдает, что для того, чтобы расплавить лед, недостаточно нагреть его до температуры плавления, т.е. до 0+1 0С, а требуется некоторое дополнительное количество теплоты, чтобы вода сменила свое агрегатное состояние. Он же в 1772 г. обнаружил, что вода имеет максимальную плотность не при температуре замерзания в 0 0С, а при +4 0С.
1766—1783 гг. оказались этапными в изучении химии воды. Последовательно химики получили водород, кислород, а затем разложили на эти газы (тогда их называли и эластичными жидкостями) воду. Для описания этих и последующих работ будем применять принятые в химии обозначения.
В 1766 г. английский физик Генри Кавендиш (1731—1810) описывает открытый им газ, который он назвал «легковоспламеняющимся воздухом» – это был водород. Водород Н 2выделялся при действии разбавленной серной H 2SO 4или соляной HCl кислоты на металлы, в частности на железо Fe, цинк Zn. Возможна такая реакция:
Fe + H 2SO 4= FeSO 4+ H 2
В 1770 г. французский ученый Антуан Лоран Лавуазье (1743—1794), исследуя предполагаемое ван Гельмонтом превращение воды в землю, приходит к заключению, что суммарный вес замкнутого стеклянного сосуда и долго кипевшей в нем воды (100 дней) остается неизменным, а земля (осадок) образуется из стекла сосуда. Для опыта Лавуазье применил дождевую воду, которую очистил восьмикратной перегонкой – дистилляцией.
В 1771 (или в 1772) г. английский химик Джозеф Пристли (1733—1804) получил кислород O 2путем нагрева селитры КNO 3. Его опыт соответствует такой реакции:
2КNO 3+ (нагрев) = 2КNO 2+ O 2
Пристли посчитал выделявшийся в указанном опыте газ за обычный воздух, в 1773 г. он видит в нем закись азота N 2O (это «веселящий газ»), которую он получил при реакции влажных железных опилок и окиси азота («азотистого воздуха»), но в 1774 г. Пристли понял, что ему удалось получить «дефлогистированный воздух» – кислород.
Этому выводу предшествовал другой опыт Пристли, проведенный 1 августа 1774 г., схема которого приведена на рис 2.
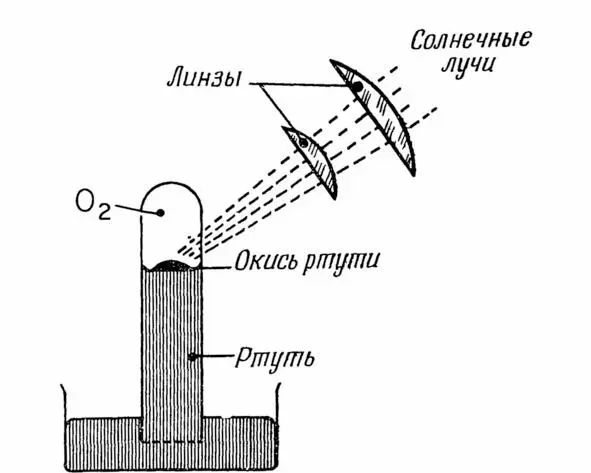
Рис. 2
С помощью двойной линзы Пристли фокусировал солнечные лучи на красный окисел ртути HgO, его сильный нагрев приводил к выделению металлической ртути Hg в виде шариков, которые стекали на ртутный столбик, и газа, заполнявшего стеклянную пробирку и оказавшегося кислородом O 2.Его опыт соответствует такой реакции:
Читать дальше













