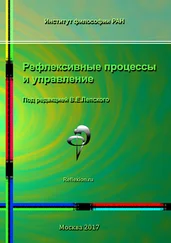
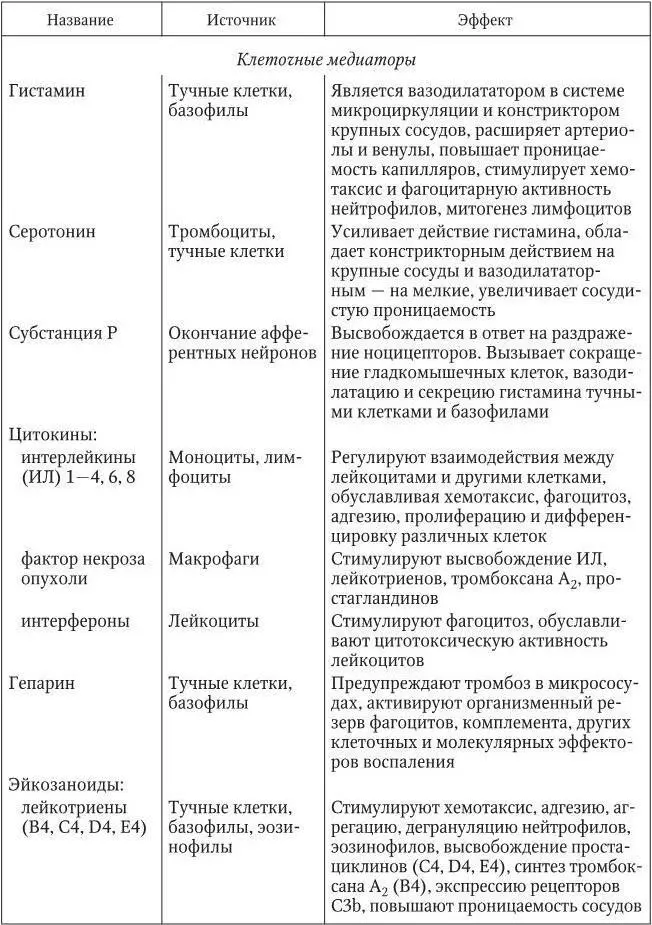
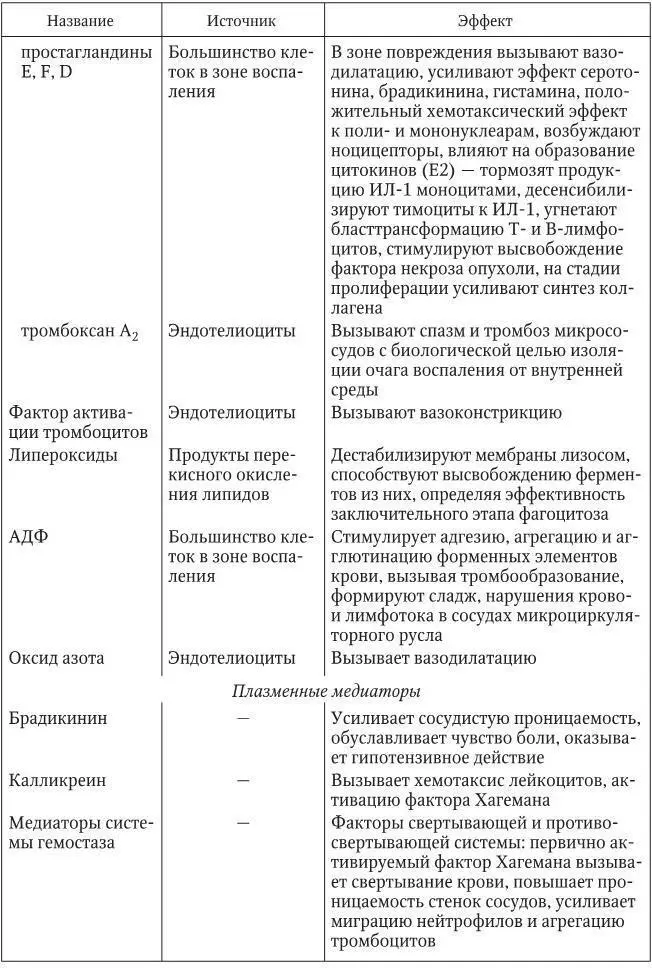
Таблица 1
Основные медиаторы воспаления(Литвицкий П. Ф., 2007)

Аналогия заключается не только в том, что обмен веществ в очаге воспаления резко повышен, но и в том, что «горение» происходит не до конца, а с образованием недоокисленных продуктов (полипептиды, жирные кислоты, кетоновые тела), обуславливающих развитие ацидоза.
Продукты первичной альтерации и клетки – участницы воспаления могут вызвать вторичное самоповреждение тканей, получившее название вторичной альтерации. Изменения микроциркуляции в очаге воспаления и прилежащих к нему тканях обуславливают значительное падение напряжения кислорода (Попов В. А., 2003). Гипоксия и связанный с ней гипоэргоз клеточных элементов вызывают развитие гипоксического тканевого некробиоза, который под действием агентов вторичной альтерации переходит в некроз, получивший название вторичного.
Вторичные повреждения тканей могут происходить по кислородзависимому (активные формы кислорода) и кислороднезависимому (гидролитические ферменты, конечный продукт активации комплемента) механизмам.
Кислородзависимые повреждения связаны с массивным образованием лейкоцитами активных кислородных радикалов, приводящих к активации процессов перекисного окисления липидов (ПОЛ) плазмы крови и клеточных мембран. Показано, что в основе формирования вторичных повреждений тканей в зоне воспаления, особенно в случае огнестрельных и гнойных ран, лежит состояние «окислительного стресса», сущностью которого является активация процессов перекисного окисления липидов на фоне нарушения функционирования системы эндогенной антиоксидантной защиты. Образующиеся при этом активные формы кислорода (АФК) и перекиси, нарастающий протеолиз и местный ацидоз усиливают деструкцию клеток, дистрофические процессы, приводя к увеличению объема повреждения, формированию вторичных некрозов, усилению микроциркуляторных расстройств. Среди АФК наиболее важное значение имеют супероксиданион-радикал (O 2 •−), гидроксилрадикал (•ОН), пергидроксильный радикал (НOO•), пероксил-радикал (RОО•) и молекулярный синглетный кислород ( 1О 2). Повреждающие ткани АФК образуются в течение первых часов и достигают своего пика на 4—5-е сутки.
Следует отметить, что уже с момента образования раневого дефекта происходит существенное уменьшение активности сбалансированной эндогенной антиоксидантной системы (АОС). Активность ферментативных и неферментативных компонентов АОС (супероксиддисмутазы, каталазы, глутатионпероксидазы, глутатион-S-трансферазы, аскорбиновой кислоты, витамина А и глутатиона) в условиях неинфицированных ран снижается на 60—70 % в течение первых 7 дней с восстановлением показателей лишь к 14-м суткам. В то же время количество продуктов ПОЛ (малоновый диальдегид) находится на высоком уровне в первые дни и снижается лишь через 14 суток.
Основным кислороднезависимым агентом вторичной альтерации являются гидролитические ферменты, высвобождаемые при некробиотической гибели клеток и при экзоцитозе. Они способны разрушать компоненты межклеточного вещества и клеточные элементы соединительной ткани. Нейтральные протеазы (коллагеназа, эластаза, катепсины, желатиназы) разрушают коллаген, эластин, базальные мембраны. Кислые протеазы вызывают деструкцию гликопротеидов и протеогликанов основного вещества соединительной ткани. Однако известно, что лизосомальные ферменты не способны сами разрушать интактную клеточную стенку и являются потенцирующими веществами более мощных агентов альтерации, а именно активных форм кислорода. Данный факт был подтвержден A. U. Grune (1997), который в своей работе показал, что в присутствии АФК более чем в 50 раз увеличивается активность протеаз.
Помимо гидролитических ферментов к кислороднезависимым факторам относят фактор некроза опухолей, катионные антибиотические белки, лактоферрин, систему комплемента.
Таким образом, среди агентов вторичной альтерации наиболее значимыми в формировании вторичных повреждений являются АФК и гидролитические ферменты. Причем цитотоксическое действие, главным образом, обусловлено АФК, которые за счет индукции ПОЛ приводят к образованию высокомолекулярных хемотаксических факторов, стимулирующих активную миграцию микро- и макрофагов. В результате этого в очаге воспаления накапливаются возбужденные лейкоциты, продуцирующие кислородные радикалы. Одновременно включаются кислороднезависимые механизмы, среди которых наиболее важную роль играют гидролитические ферменты лизосом (нейтральные и кислые протеазы, липазы, гликозидазы). В условиях грубого нарушения гомеостаза, микро- и макроциркуляции, истощения антиоксидантной защиты активация кислородзависимых и кислороднезависимых механизмов вторичной альтерации ведет сначала к расширению территории очага воспаления за счет окружающих тканей, а затем к их повреждению и гибели. Поэтому объем зоны вторичного повреждения всегда больше, чем первичного (Попов В. А., 2003). Так, исследование объема некротических тканей, удаляемых при первичной и вторичной хирургической обработке, показало, что масса погибших тканей за счет вторичного некроза превышает или равна массе некротических тканей, удаляемых при первичной хирургической обработке.
Читать дальше
Конец ознакомительного отрывка
Купить книгу