Чтобы закончить наши рассуждения о химической природе стекла и тех веществах, из которых оно образуется, приведем примерные составы некоторых типичных промышленных стекол (табл. 1).
Беглого взгляда на приведенные рецепты достаточно, чтобы убедиться в разнообразии комбинаций, составляемых из небольшого количества стеклообразующих окислов. Этот перечень рецептов можно увеличить в десятки раз. Одни оптические стекла охватывают собой несколько сот сортов, из которых каждый обладает какими-то особенными свойствами и имеет свой состав. отличающий его от всех других стекол.
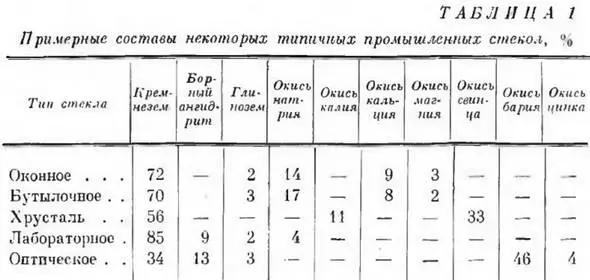
Таким образом, разнообразные требования к свойствам стекла на практике удовлетворяются различными комбинациями нескольких входящих в состав стекол окислов. Иногда этих окислов в состав стекла входит очень мало (но не меньше трех), иногда — до десяти. Содержание главной составной части стекла — кремнезема — колеблется от 85 до 35%, а щелочей, т. е. окислов натрия и калия, — от 17% почти до нуля. Такие вещества, как окись бария и окись свинца, иногда совершенно отсутствуют, а иногда содержание их в стекле поднимается до 30-45% и выше [1] Здесь не предусматриваются стекла особых составов.
.
Все ото лишний раз подтверждает, что химический состав — могущественное средство, которым пользуются для придания материалу нужных свойств.
Итак, мы имеем достаточно полное представление о природе стекла, о его свойствах и о химических соединениях, входящих в его состав.
Познакомимся теперь с условиями его приготовления.
Как уже говорилось раньше, для того чтобы из смеси сырых материалов — шихты — получилось стекло, ее необходимо подвергнуть действию высокой температуры. При этом первой расплавится щелочь, после чего в ней начнут растворяться зерна кварца и известняка, вступая между собой в химическое соединение с образованием различных, растворенных друг в друге силикатов.
В результате по истечении нескольких часов при температуре около 1400-1500° получается расплав, в котором уже не осталось ни одной крупинки исходных материалов. Этим заканчивается первая стадия варки стекла, называемая «проваром шихты». Расплав представляет собой прозрачное вещество и уже может быть назван стеклом, так как при охлаждении он сохранит свою прозрачность и не будет обнаруживать признаков кристаллического строения, присущего всем исходным материалам, входившим в шихту.
Однако этот расплав еще не является готовым стеклом, из которого можно формовать изделия. Он недостаточно однороден. В нем имеется громадное количество пузырьков и так называемых «свилей» — нитеобразных потоков. Пузырьки бывают разной величины — от одного сантиметра до сотых в даже тысячных долей миллиметра в диаметре. Самые мелкие из них называются «мошкой». Пузырьки наполнены воздухом и газами, находящимися в продуктах горения, а также выделяющимися из шихты при диссоциации ее компонентов под влиянием высоких температур. Удаление пузырьков из расплава благодаря его большой вязкости представляет собой очень трудную задачу, не всегда удающуюся до конца.
На рис. 1 показаны пробы, последовательно извлекаемые из расплава по мере протекания процесса стеклообразования и характеризующие разные стадии варки стекла.
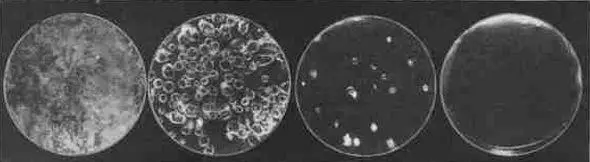
Рис.1. Стадии варки стекла
Свиль — это видимая граница двух соседних участков стекла неодинакового состава; она является признаком недостаточной однородности, недостаточно хорошей перемешанности расплава (рис. 2). Аналогичную картину свилистости мы можем наблюдать в стакане чая, когда в нем растворяется кусок сахара. При этом нетрудно заметить клубок нитевидных потоков, который будет подниматься над сахаром до тех пор, пока сахар не растает и чай не будет как следует перемешал ложкой.

Рис. 2. Свили в стекле
Чтобы пузырьки и связи удалились из расплавленного стекла, его нужно выдержать в течение нескольких часов при высоких температурах. Этот второй этап варки стекла называется «осветлением». Расплав будет постепенно разогреваться и становиться все более и более жидким, что облегчит удаление пузырей, так как скорость их подъема в жидкости обратно пропорциональна ее вязкости, и поможет уничтожению свилей, так как расплав будет лучше перемешиваться.
Читать дальше















