Первым в таблице стоит водород (Н) с атомным весом, примерно равным единице. Далее в тот же период входит гелий (Не), которым и заканчивается самый короткий, первый, период. Затем начинается второй период, включающий восемь элементов: литий (Li), бериллий (Be), бор (В), углерод (С), азот (N), кислород (О), фтор (F) и неон (Ne). Следующий, третий, период также включает восемь элементов. Это три так называемых малых периода.
Вслед за ними идут большие периоды, каждый из которых включает по 18 элементов (четвертый и пятый периоды). Сначала считалось, что и в следующих периодах содержится также по 18 элементов. Впоследствии оказалось, что при этом большое число открытых позже элементов (так называемые редкоземельные металлы, или лантаниды; от элемента 57 до элемента 71) приходится все включать в одну клетку таблицы. Таким образом, следующий период включает на 18+14=32 элемента. Все эти сложные дополнительные обстоятельства были не только обнаружены, но и получили впоследствии исчерпывающее объяснение. Такое объяснение было дано уже в нашем столетии, в основном после смерти Менделеева. Периодический закон, как и ряд других великих открытий XIX века, не только обобщил и объяснил множество ранее известных фактов, но и поставил перед следующим столетием новые коренные вопросы. В самом конце XIX столетия периодическая система после триумфальных открытий 70–80-х годов (Лекок де Буабодран, Нильсен, Винклер) выдержала серьезное испытание. Как уже говорилось, к открытому в 1894 году не вмещавшемуся в таблицу Менделеева аргону в последующие годы прибавились другие инертные газы — гелий, неон, криптон и ксенон, образовавшие новую, нулевую, группу элементов. Теперь таблица состояла из девяти групп (0, I, II, III, IV, V, VI, VII, VIII). Менделеев придал ей сравнительно простой вид, разделив каждый длинный период на два коротких. Это было сделано еще в 1871 году; после же открытия инертных газов «короткая» таблица получила несколько новый вид (см. таблицу на стр. 49).
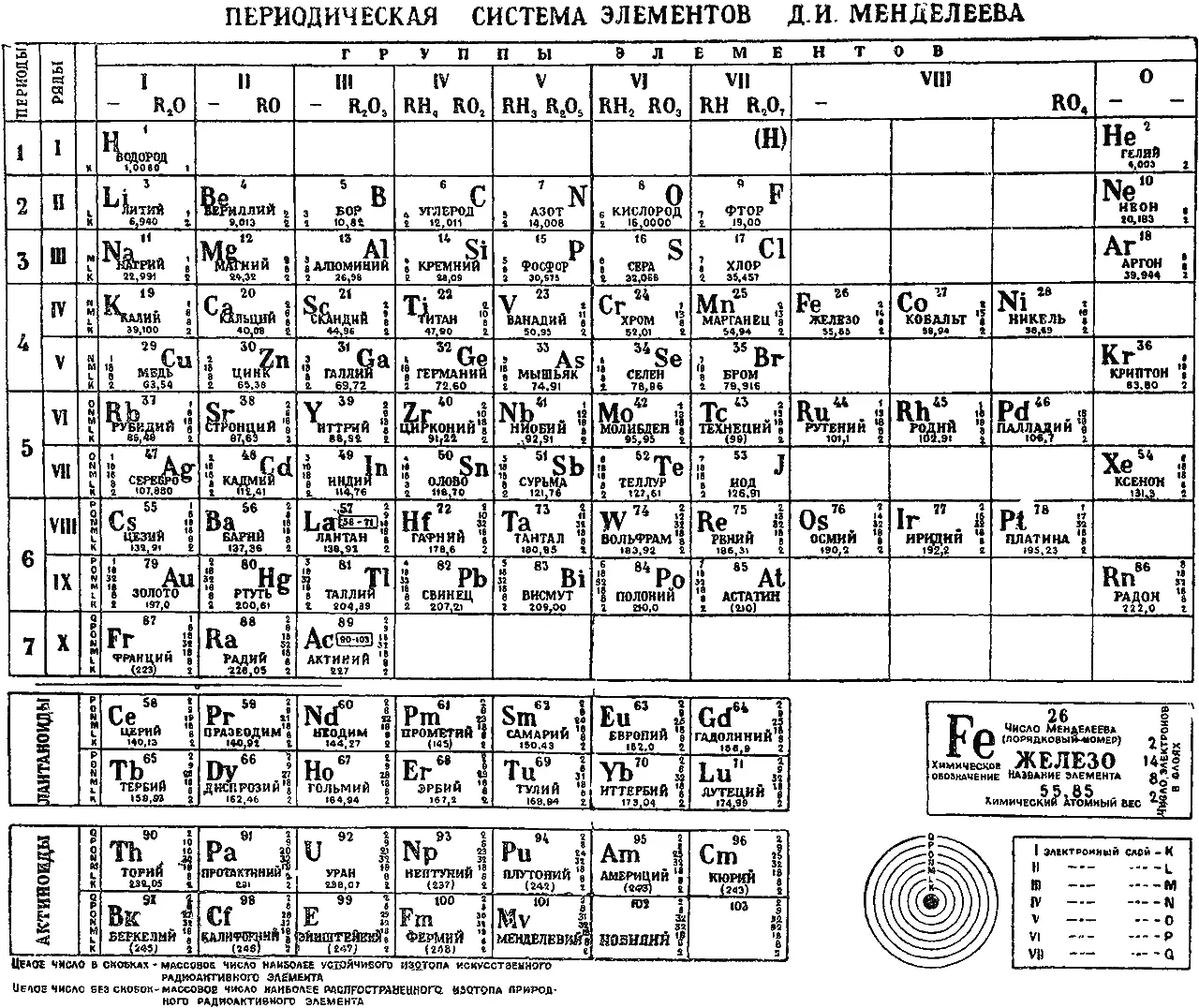
Что же оставалось неясным в этой таблице? Какие вопросы ставила она перед дальнейшим развитием науки?
Прежде всего в таблице оставались свободные клетки. С другой стороны, ряд различных элементов (лантаниды) помещался в одной клетке. Но главный вопрос состоял в самой периодичности. Почему свойства элементов периодически повторяются, если элементы расположить в порядке возрастания их атомного веса. Отвечая на этот вопрос, физика XX века ответила и на многие другие столь же важные вопросы, поставленные перед ней периодической системой.
ПЕРИОДИЧЕСКИЙ ЗАКОН И СТРОЕНИЕ АТОМА
Открытие Менделеева было одним из исходных пунктов развития новейшей физики, раскрывшей внутреннее строение атома и атомного ядра, освободившей атомную энергию и достигшей других замечательных успехов. В конце XIX и начале XX века физики открыли элементарные частицы, входящие в состав атомов, обнаружив таким образом сложную природу атома. Первоначально были найдены электроны — частицы, обладающие очень малой массой и отрицательным электрическим зарядом, равным единице [8] Заряд электрона, равный 4,810 -10 CGSE, обычно принимается за единицу измерения величины заряда в атомной физике.
. Впоследствии были обнаружены гораздо более тяжелые (в 1836 раз тяжелее электрона) положительно заряженные частицы — протоны, электрически незаряженные частицы — нейтроны, а также ряд других элементарных частиц.
Исследование структуры атома и атомного ядра, а также открытие входящих в состав ядер элементарных частиц было тесно связано с изучением явлений радиоактивности. В 1896 году французский физик Анри Беккерель, исследуя свечение тел, пришел к важному открытию. Соли урана заставляли чернеть фотографическую пластинку, что свидетельствовало об излучении. Это ранее неизвестное излучение было названо радиоактивностью. Один из крупнейших физиков Франции Пьер Кюри и его жена уроженка Варшавы, Мария Склодовская-Кюри, изучая соединения урана, обнаружили, что смоляная урановая руда, «смоляная обманка», полученная из Чехии, отличается сильным радиоактивным излучением, бóльшим, чем даже чистый уран. Они предположили, что в этой руде имеется некий элемент, обладающий большей радиоактивностью, чем уран. В 1898 году им удалось выделить этот элемент. Действительно, оказалось, что он дает излучение в миллион раз более интенсивное, чем уран. Этот элемент был назван радием. Он испускает различного рода лучи, в том числе поток положительно заряженных частиц — альфа-лучи. Причиной излучения является распад ядер атомов радия. Уран также распадается, но так медленно, что только через 4,6 миллиарда лет его количество уменьшится вдвое. При распаде урана образуется открытый Марией Склодовской и Пьером Кюри радий. Его распад происходит быстрее, так что количество радия уменьшится вдвое примерно через 1590 лет.
Читать дальше








