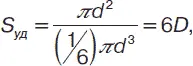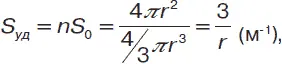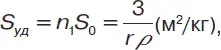По степени дисперсности обычно выделяют следующие классы дисперсных систем.
Грубодисперсные системы– системы, размер частиц дисперсной фазы в которых превышает 10 –3см.
Микрогетерогенные системы– размер частиц колеблется от 10 –5до 10 –3см.
Ультрамикрогетерогенные системы– размер частиц колеблется от 10 –7до 10 –5см; их называют также высокодисперсными, или коллоидными, системами. Коллоидные системы характеризуются гетерогенностью, т. е. наличием поверхностей раздела фаз и очень большим значением удельной поверхности дисперсной фазы. Высокодисперсные системы обычно называют золями. Иногда выделяют молекулярно-дисперсные(ионно-дисперсные) системы, которые, строго говоря, являются истинными растворами, т. е. гомогенными системами, поскольку в них нет поверхностей раздела фаз. По структуре все дисперсные системы подразделяют на свободнодисперсные, в которых частицы дисперсной фазы не связаны между собой (суспензии, эмульсии, золи), и связанодисперсные, в которых одна из фаз структурно закреплена (гели, пены). Дисперсные системы подразделяют на две группы, отличные по характеру межфазных взаимодействий между частицами дисперсной фазы и дисперсионной среды. В зависимости от этого они могут быть лиофобнымиили лиофильными. Для них характерно слабое межмолекулярное взаимодействие вещества дисперсной фазы со средой, а для вторых – сильное. Это взаимодействие приводит к образованию сольватных (в случае воды – гидратных) оболочек из молекул дисперсионной среды вокруг частиц, процесс называется сольватацией (гидратацией). К лиофобным коллоидам относятся системы, в которых частицы дисперсной фазы слабо взаимодействуют с дисперсионной средой; эти системы могут быть получены только с затратой энергии и устойчивы лишь в присутствии стабилизаторов. Лиофобные и лиофильные дисперсные системы различаются также структурой частиц, составляющих дисперсную фазу. Для лиофобных коллоидов единицей структуры является сложный многокомпонентный агрегат переменного состава – мицелла, для лиофильных растворов – макромолекула.
4. Дисперсность. Удельная поверхность дисперсных систем, методы ее измерения
Основная характеристика дисперсных систем – размеры частиц, или дисперсность.Дисперсные системы делят на грубодисперсные (низкодисперсные) и тонкодисперсные (высокодисперсные), или коллоидные системы(коллоиды). В грубодисперсных системах частицы имеют размер от 10 –4см и выше, в коллоидных – от 10 –4до 10 –5– 10 –7см. Дисперсность определяется по трем измерениям тела, либо характеризуется величиной, обратной минимальному размеру и названной дисперсностью, либо через удельную площадь поверхности S уд(отношение межфазной поверхности к объему тела). Количественной характеристикой дисперсности (раздробленности) вещества является степень дисперсности (степень раздробленности D ) – величина, обратная размеру дисперсных частиц а: D = 1/ a , где а равно диаметру сферических или волокнистых частиц, или длине ребра кубических частиц, или толщине пленок. Все частицы дисперсной фазы имеют одинаковые размеры – монодисперсная система. Частицы дисперсной фазы неодинакового размера – полидисперсная система. Соотношение между поверхностью и объемом характеризует удельная поверхность:
S уд= S / V .
Для частиц сферической формы она равна:
S уд= 4 πr 2/ (4 / 3 πr ) = 3 / r = 6 / d .
Для частиц кубической формы –
S уд= 6 l 2/ l 3= 6 / l ,
где r – радиус шара; d – его диаметр; l – длина ребра куба.
Дисперсность D связана с удельной поверхностью S уд:
S уд = S / V = k / d = kD,
где V – объем дисперсной фазы, мл.
Для сферических частиц уравнение принимает вид:
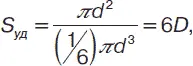
k – коэффициент формы частиц; d – диаметр частицы, м 2.
Формула для расчета удельной поверхности ( S уд) системы с шарообразными частицами:
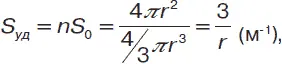
где n – число частиц, м 3; S 0– поверхность каждой частицы.
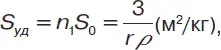
где n 1– число частиц, кг; r – плотность вещества, г/см 3.
Читать дальше