Надо сказать, что в общих чертах идея топливных элементов зародилась давно, более 100 лет назад. Однако осуществить ее оказалось гораздо сложнее, чем предполагали вначале. Лишь многолетнее развитие электрохимической теории, достижения металлургии, автоматики и других отраслей науки и техники позволили в последние годы создать топливные элементы, пригодные для практического использования.
Горение без пламени
Полыхает костер, бушует в печи пламя… Каждый повседневно встречается с таким горением и знает, что оно сопровождается высокой температурой. А химик добавит, что при подобном химическом горении происходит окислительно-восстановительный процесс между горючим веществом (топливом) и окислителем (кислородом). При этом атомы топлива окисляются, то есть теряют электроны, а атомы окислителя восстанавливаются — наоборот, приобретают электроны.
Такие окислительно-восстановительные процессы характеризуются случайным перемещением атомов и молекул окислителя и топлива, между которыми идет непрерывный обмен электронами. Что это значит с энергетической точки зрения?
Известно, что энергетический уровень атомов определяется строением их внешней электронной оболочки, которая может иметь определенное количество электронов. Атомы горючих и окислительных веществ имеют внешние оболочки, заполненные электронами не полностью. Если взять горючим водород, то у него на внешней оболочке «недостает» одного электрона, хотя оболочка позволяет иметь два. В атоме же окислителя — кислорода «не хватает» двух электронов (до восьми). Заполнение внешней оболочки электронами вызывает уменьшение энергетического уровня атома. Таким образом, обмен электронами между атомами топлива и окислителя в процессе горения можно рассматривать как переход электронов с высшего энергетического уровня на низший. А он сопровождается высвобождением энергии в виде тепла, которое, как уже было сказано, невозможно полностью обратить в полезную работу
Важно отметить и другое. Поскольку обмен электронами при химическом горении происходит хаотично — с различными скоростями и в различных направлениях, — возникновение электрического тока исключается. Тут, если так можно выразиться, идет процесс бесчисленного множества «коротких замыканий» между атомами и молекулами, имеющими различные электрические потенциалы.
Другое дело, если исключить хаотическое перемещение электронов, сообщить им направленное движение. Тогда энергия реакции почти полностью пойдет на образование электрической энергии. Химическое горение топлива с высокой температурой, таким образом, превратится в холодное, электрохимическое. В горение без пламени. Именно оно и используется в топливных элементах для получения постоянного электрического тока.
Топливный элемент во многом напоминает обычный гальванический: те же два специально обработанных металлических электрода, разделенные электролитом. Отличие в том, что к одному электроду топливного элемента непрерывно подводится топливо, а к другому — окислитель, и так, что исключена возможность их смешивания.
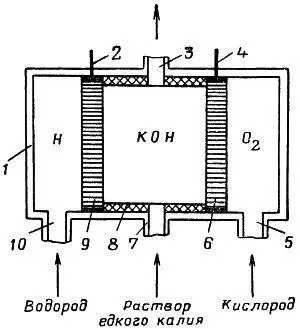
Рис. 11. Принципиальная схема устройства водородно-кислородного топливного элемента:
1 — корпус; 2 и 4 — выводы электродов; 5 — канал для подвода кислорода; 6 и 9 — электроды; 7 и 3 — каналы для электролита; 8 — изоляционная прокладка; 10 — канал для подвода водорода
Принципиальное устройство топливного элемента удобно проиллюстрировать на водородно-кислородном элементе (рис. 11). Пространство корпуса 1 разделяется электродами 6 и 9. По каналу 10 в пространство Н подается водород — топливо, а по каналу 5 в пространство О 2подается кислород — окислитель. Через каналы 7 и 5 пропускается электролит — концентрированный раствор едкого калия (КОН).
На кислородном электроде 6 кислород поглощается. В результате процессов его взаимодействия с водой, находящейся в электролите, и электронами из металла электрода образуются ионы гидроксильной группы ОН. Кислородный электрод, потерявший электроны и оказавшийся обедненный ими, принимает положительный потенциал.
На водородном электроде 9 поглощается водород. Он переходит из молекулярного состояния в атомарное. Поглощенные атомы ионизируются и переносятся в электролит, оставляя электроны на электроде. Водородный электрод оказывается обогащенным электронами и принимает отрицательный потенциал.
Читать дальше













