Перейдем теперь к другому процессу. На фиг. 1.6 мы видим, как (с атомной точки зрения) соль растворяется в воде.
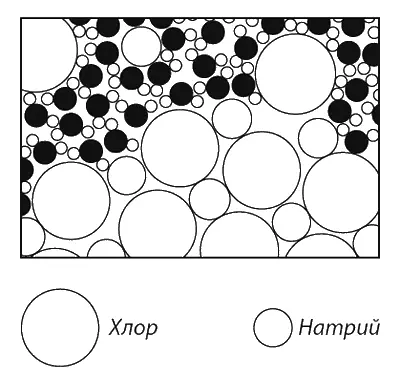
Фиг. 1.6. Молекулы соли, растворяющейся в воде.
Что получается, если в воду бросить кристаллик соли? Соль – твердое тело, кристалл, в котором «атомы соли» расставлены правильными рядами. На фиг. 1.7 показано трехмерное строение обычной соли (хлористого натрия).
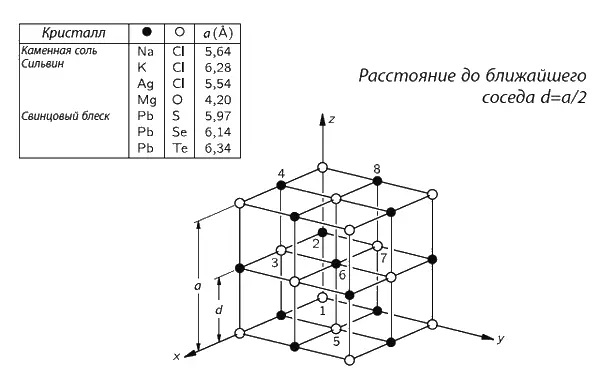
Фиг. 1.7. Структура кристалла соли.
Строго говоря, кристалл состоит не из атомов, а из ионов . Ионы – это атомы с излишком или с нехваткой электронов. В кристалле соли мы находим ионы хлора (атомы хлора с лишним электроном) и ионы натрия (атомы натрия, лишенные одного электрона). Ионы в твердой соли скреплены друг с другом электрическим притяжением, но в воде некоторые из них, притянувшись к положительному водороду или отрицательному кислороду, начинают свободно двигаться. На фиг. 1.6 виден освободившийся ион хлора и другие атомы, плавающие в воде в виде ионов. На рисунке нарочно подчеркнуты некоторые детали процесса. Заметьте, например, что водородные концы молекул воды обычно обступают ион хлора, а возле иона натрия чаще оказывается кислород (ион натрия положителен, а атом кислорода в молекуле воды отрицателен, поэтому они притягиваются). Можно из рисунка понять: растворяется здесь соль в воде или же выкристаллизовывается из воды? Ясно, что нельзя; часть атомов уходит из кристалла, часть присоединяется к нему. Процесс этот динамический , подобный испарению; все зависит от того, много или мало соли в воде, в какую сторону нарушено равновесие. Под равновесным понимается такое состояние, когда количество уходящих атомов равно количеству приходящих. Если в воде почти нет соли, то больше атомов уходит в воду, чем возвращается из воды: соль растворяется. Если же «атомов соли» слишком много, то приход превышает уход и соль выпадает в кристаллы.
Мы мимоходом упомянули, что понятие молекулы вещества не совсем точно и имеет смысл только для некоторых видов веществ. Оно применимо к воде, в ней действительно три атома всегда скреплены между собой, но оно не очень подходит к твердому хлористому натрию. Хлористый натрий – это ионы хлора и натрия, образующие кубическую структуру. Нельзя естественным путем сгруппировать их в «молекулы соли».
Вернемся к вопросу о растворении и осаждении соли. Если повысить температуру раствора соли, то возрастет и число растворяющихся атомов и число осаждаемых. Оказывается, что в общем случае трудно предсказать, в какую сторону сдвинется процесс, быстрей или медленней пойдет растворение. С ростом температуры большинство веществ начинает растворяться сильней, а у некоторых растворимость падает.
Во всех описанных процессах атомы и ионы не меняли своих напарников. Но, конечно, возможны обстоятельства, в которых сочетания атомов меняются, образуя новые молекулы. Это показано на фиг. 1.8. Процесс, в котором атомные партнеры меняются местами, называется химической реакцией . Описанные нами прежде процессы называются физическими, но трудно указать резкую границу между теми и другими. (Природе все равно, как мы это назовем, она просто делает свое дело.) На картинке мы хотели показать, как уголь горит в кислороде. Молекула кислорода состоит из двух атомов, сцепленных очень крепко. (А почему не из трех или даже не из четырех ? Такова одна из характерных черт атомных процессов: атомы очень разборчивы, им нравятся определенные партнеры, определенные направления и т. д. Одна из обязанностей физики – разобраться, почему они хотят именно то, что хотят. Во всяком случае два атома кислорода, довольные и насыщенные, образуют молекулу.)
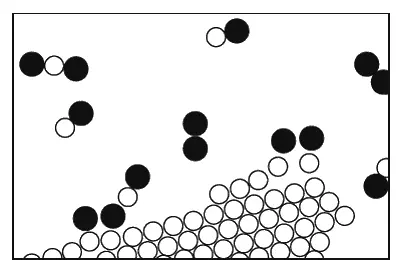
Фиг. 1.8. Уголь, горящий в кислороде.
Предположим, что атомы углерода образуют твердый кристалл (графит или алмаз [1] Алмаз тоже может сгореть в воздухе.
). Одна из молекул кислорода может пробраться к углероду, каждый ее атом подхватит по атому углерода и улетит в новом сочетании углерод – кислород. Такие молекулы образуют газ, называемый угарным. Его химическое имя СО. Что это значит? Буквы СО – это фактически картинка такой молекулы: С – углерод, О – кислород. Но углерод притягивает к себе кислород намного сильнее, чем кислород притягивает кислород или углерод – углерод. Поэтому кислород для этого процесса может поступать с малой энергией, но, схватываясь с неимоверной жадностью и страстью с углеродом, высвобождает энергию, поглощаемую всеми соседними атомами. Образуется большое количество энергии движения (кинетической энергии). Это, конечно, и есть горение; мы получаем тепло от сочетания кислорода и углерода. Теплота в обычных условиях проявляется в виде движения молекул нагретого газа, но иногда ее может быть так много, что она вызывает и свет . Так получается пламя.
Читать дальше
![Ричард Фейнман Фейнмановские лекции по физике. Современная наука о природе [litres] обложка книги](/books/398001/richard-fejnman-fejnmanovskie-lekcii-po-fizike-sov-cover.webp)








![Пол Халперн - Квантовый лабиринт. Как Ричард Фейнман и Джон Уилер изменили время и реальность [litres]](/books/414310/pol-halpern-kvantovyj-labirint-kak-richard-fejnman-thumb.webp)
