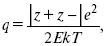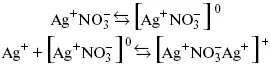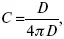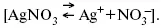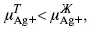Параметр Бьеррума
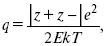
где е – заряд электрона –16 x 10– 19Кл;
к – константа Больцмана = 1.38 x 10– 23Кдж/к;
Т – абсолютная температура;
Е – диэлектрическая проницаемость.
Ассоциация ионов– образование из противоположно заряженных ионов (в растворах электролитов) особого рода частиц-ассоциатов, в которых ионы удерживаются за счет электростатического взаимодействия их электрических зарядов в соответствии с законом Кулона. Процессы ассоциации ионов подчиняются закону действующих масс, термодинамическим соотношениям.
Простейшие ассоциаты– ионные пары, нейтральные или электрически заряженные, термодинамически устойчивые частицы, находящиеся в равновесии с простыми ионами.
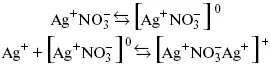
Степень ассоциации ионов зависит от природы растворителя, электролита, температуры, концетрации раствора. Она возрастает с уменьшением диэлектрической проницаемости растворителя вследствие увеличения кулоновского притяжения ионов.
Ассоциация– объединение однородных частиц в растворе.
Сольватация– взаимодействие растворенного вещества с растворителем. Молекулярные группы, сольваты, образовавшиеся в результате взаимодействия, слой молекул растворителя, связанный с центральной частицей сольвата силами притяжения – сольватная оболочка.Наименьшее число молекул, удерживаемых в непосредственной близости от сольватированной частицы – координационное число сольватации. В зависимости от природы растворенного вещества, сольваты могут образовываться различными путями. Ион-дипольное взаимодействие– при растворении веществ с ионной структурой молекулы растворителя удерживаются около иона силами электростатического притяжения. Процесс гидратации– взаимодействие веществ с водой.
2. Термодинамика растворов электролитов. Типы ДЭС
На границе раздела фаз электрод – раствор происходит перераспределение зарядов, в результате которого у поверхности электрода накапливается избыток ионов какого-либо одного знака, в результате на поверхности возникает избыток зарядов противоположного знака. Такое пространство разделения избыточных зарядов позволяет ввести понятие ДЭС. Условно можно представить две воображаемые плоскости, которые проходят через центры тяжести избыточных зарядов в поверхностном слое на электроде и раствора у поверхности электрода.
Расстояние между плоскостями равно диаметру сольватированного комплекса (d). Таким образом, ДЭС можно рассматривать как плоский конденсатор:
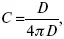
D – диэлектрическая проницаемость, для Н 2О = 80, d = 10– 8– расстояние между обкладками. Перераспределяемый заряд на границе раздела фаз имеет динамическое преобладание.
Согласно закону термодинамики, перенос вещества из одной фазы в другую характеризуется химическим потенциалом
μ = Δ G хим
μ зависит от концентрации частиц.
μ = μ 0 +RT ln С,
где С – концентрация частиц, участвующих в реакции переноса;
μ 0– стандартное значение потенциала при С= 1.
Согласно термодинамике, перенос вещества из одной фазы в другую происходит таким образом, что химический потенциал вещества действует до тех пор, пока μ 1= μ 2 в обеих фазах.
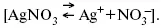
Определяющимися ионами являются ионы Ag +, следовательно, если химический μ ионов Ag (Ме),
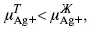
то, согласно уравнению Ле-Шателье, перенос ионов Ag +, в сторону раствора будет происходить с большей скоростью, чем в обратном направлении, в результате количество ионов Ag у поверхности будет увеличиваться, так как концентрация в растворе растет.
μ Ag+= μ 0+ RT lnC Ag+.
Перенос происходит до тех пор, пока
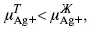
Когда наступит равенство μ , скорость переноса в обоих направлениях через границу раздела фаз становится одинаковой.
Наступает равновесие; так как в переносе принимают участие заряженные частицы, то в этом случае говорят об электрохимическом равновесии. При установлении равновесия поверхность, с которой ушли Ag +, приобретает избыток отрицательного заряда, под действием его избыток положительных зарядов собирается в растворе у поверхности.
Читать дальше
Конец ознакомительного отрывка
Купить книгу