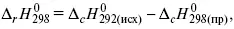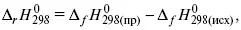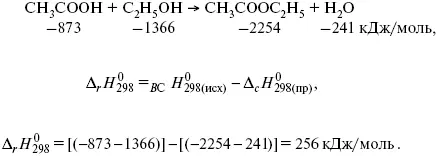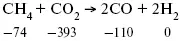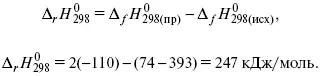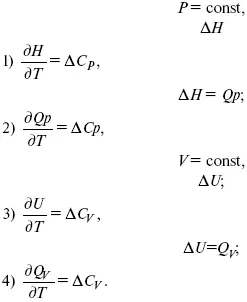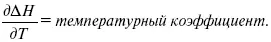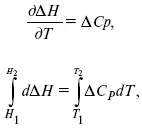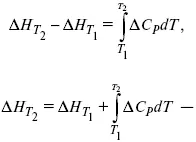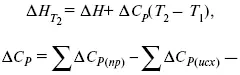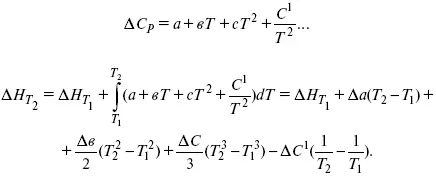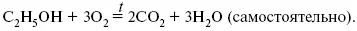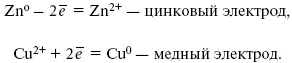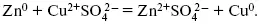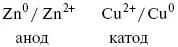δ Q P= dH,
δ Q V= dU вн,
Q P= Δ H,
Q V= Δ U вн.
Современная формулировка закона Гесса– общие приращения энтальпии при переходе начальных веществ в продукты реакции не зависят от того, через какие промежуточные стадии прошла реакция.
Закон Гесса позволяет рассчитать тепловые эффекты или приращение энтальпии только при стандартных условиях ( р = 1 атм = 10 5Па, Т = 273 К + 25 = 298 К).
Теплоты при стандартных условиях сведены в таблицу (справочник под редакцией Нищенко). Для индивидуальных веществ: С, Н 2, Fe и др. – Δ Н = 0.
Следствия из закона Гесса:
1) энтальпия образования 1 моля соединения из простых веществ не зависит от способа получения;
2) теплоты сгорания – «теплота реакции равна сумме теплот сгорания исходящих веществ за вычетом теплот сгорания продуктов реакции с учетом стехиометрических коэффициентов»
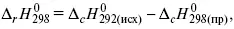
где r – реакции;
c – композиция;
3) теплоты образования – «тепловой эффект реакции равен разности между теплотами образования всех веществ, указанных в правой части уравнения (продукт реакции), и теплотами образования всех веществ, указанных в левой части уравнения».
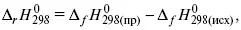
где f – формация.
Пример 1.Рассчитать тепловой эффект реакции этерификации спирта.
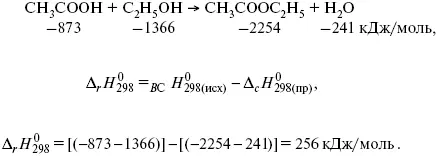
Пример 2.Рассчитать тепловой эффект реакции, протекающей по уравнению:
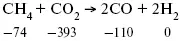
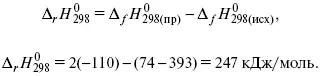
3. Закон Кирхгоффа. Интегральная форма уравнений Кирхгоффа
3акон Кирхгоффа
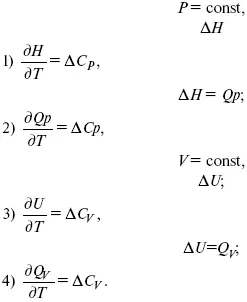
Это уравнения Кирхгоффа в дифференциальной форме.
Когда идет изменение функции по t – температурный коэффициент:
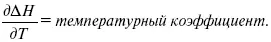
Закон Кирхгоффа:температурный коэффициент теплового эффекта равен изменению теплоемкости данного процесса.
Интегральная форма уравнений Кирхгоффа:
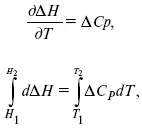
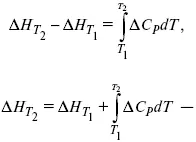
интегральная форма уравнений Кирхгоффа, Т 1 = 298 К.
1) Δ СР ≠ f(T)
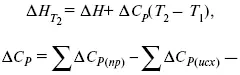
усредненное Δ Н при Т 1 – по закону Гесса;
2) Δ СР = f(T)
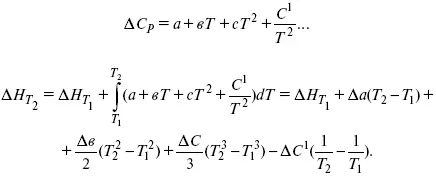
Пример 3.Рассчитать тепловой эффект химической реакции при Т= 1000 К (реакция сгорания С 2Н 5ОН).
С 2Н 5ОН + 30 2= 2С0 2+ ЗН 20 (самостоятельно).
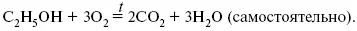
Все реакции – как реакции образования:
Т = 1000 к.
ЛЕКЦИЯ № 10. Гальванические элементы
1. Понятие гальванического элемента
Гальванический элемент– прибор, который преобразовывает химическую энергию в электрическую. Одним из таких элементов является элемент Даниэля – Якоби. Этот элемент состоит из двух электродов: цинкового и медного, – погруженных в соответствующие сульфатные растворы, между которыми пористая перегородка:
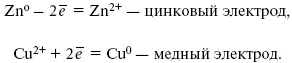
При замыкании внешней цепи электроны переходят от Zn к Cu, происходит диффузия цинка в медь:
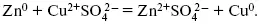
Образуем электрохимическую схему:
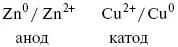
Анод – отрицательный электрод (слева). Катод – положительный электрод.
Читать дальше
Конец ознакомительного отрывка
Купить книгу