Рис. 2.1
Мы знаем, что устойчиво состояние, в котором потенциальная энергия имеет наименьшее значение. Когда атом входит в состав молекулы, он "сидит" в потенциальной яме, совершая небольшие тепловые колебания около положения равновесия.
Расстояние от вертикальной оси до дна ямы можно назвать равновесным. На этом расстоянии расположились бы атомы, если бы прекратилось тепловое движение.
Кривая потенциальной энергии рассказывает о всех деталях взаимодействия между атомами. Притягиваются или отталкиваются частицы на том или ином расстоянии, возрастает или убывает сила взаимодействия при отдалении или сближении частиц - все эти сведения можно получить из анализа кривой потенциальной энергии. Точки левее "дна" соответствуют отталкиванию. Напротив, участки кривой правее дна ямы характеризуют притяжение. Важные сведения сообщает и крутизна кривой: чем круче идет кривая, тем больше сила.
Находясь на больших расстояниях, атомы притягиваются один к другому; эта сила весьма быстро уменьшается с увеличением расстояния между ними. При сближении сила притяжения возрастает и достигает наибольшего значения уже тогда, когда атомы подойдут один к другому очень близко. При еще большем сближении притяжение ослабевает и, наконец, на равновесном расстоянии сила взаимодействия обращается в нуль. При сближении атомов на расстояние, меньшее равновесного, возникают силы отталкивания, которые очень резко нарастают и быстро делают практически невозможным дальнейшее уменьшение расстояния между атомами.
Равновесные расстояния (ниже мы будем говорить короче - расстояния) между атомами различны для разных сортов атомов.
Для разных пар атомов различны не только расстояния от вертикальной оси до дна ямы, но и глубина ям.
Глубина ямы имеет простой смысл: чтобы выкатиться из ямы, нужна энергия, как раз равная глубине. Поэтому глубину ямы можно назвать энергией связи частиц.
Расстояния между атомами молекул столь малы, что для их измерения надо выбрать подходящие единицы, иначе пришлось бы выражать их значения, например, в таком виде: 0,000000012 см. Это цифра для молекулы кислорода.
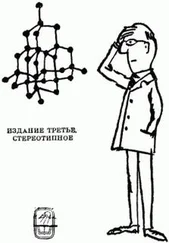
Единицы, особенно удобные для описания атомного мира, называются ангстремами (правда, фамилия шведского ученого, именем которого названы эти единицы, правильно читается Онгстрем; для напоминания об этом над буквой А ставят кружок):
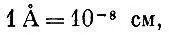
т. е. одной стомиллионной доле сантиметра.
Расстояния между атомами молекул лежат в пределах от 1 до 4Å. Написанное выше равновесное расстояние для кислорода равно 1,2 Å.
Межатомные расстояния, как вы видите, очень малы. Если опоясать земной шар веревкой у экватора, то длина "пояса" во столько же раз будет больше ширины вашей ладони, во сколько раз ширина ладони больше расстояния между атомами молекулы.
Для измерения энергии связи пользуются обычно калориями, но относят их не к одной молекуле, что дало бы, разумеется, ничтожную цифру, а к одному молю, т.е. к N Aмолекулам.
Ясно, что энергия связи на один моль, если ее поделить на число Авогадро N A=6,023*10 23моль -1, даст энергию связи одной молекулы.
Энергия связи атомов в молекуле, как и межатомные расстояния, колеблется в незначительных пределах.
Для того же кислорода энергия связи равна 116 000 кал/ моль, для водорода 103 000 кал/ мольи т. д.
Мы уже говорили, что атомы в молекулах располагаются вполне определенным образом одни по отношению к другим, образуя в сложных случаях весьма замысловатые постройки.
Приведем несколько простых примеров.
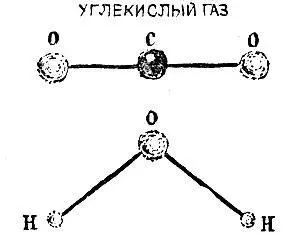
Рис. 2.2
В молекуле С0 2(углекислый газ) все три атома расположены в ряд - атом углерода посередине. Молекула воды Н 20 имеет уголковую форму, вершиной угла (он равен 105°) является атом кислорода.
В молекуле аммиака NH 3атом азота находится в вершине трехгранной пирамиды; в молекуле метана СН 4атом углерода находится в центре четырехгранной фигуры с равными сторонами, которая называется тетраэдром.
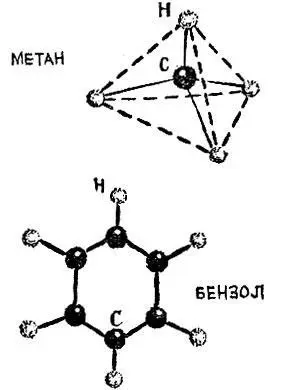
Рис. 2.3
Атомы углерода бензола С 6Н 6образуют правильный шестиугольник. Связи атомов углерода с водородом идут от всех вершин шестиугольника. Все атомы расположены в одной плоскости.
Читать дальше