
Рисунок 3. Пиранозные и фуранозные формы углеводов
3. α- и β-аномеры. При циклизации образуется гидроксильная группа при полуацетальной или полукетальной группировке, полуацетальный или полукетальный гидроксил, эта группа может располагаться под циклом, в результате образуется α-аномер, а может располагаться над циклом, тогда образуется β-аномер. Циклическая структура сохраняется и в растворе, но при этом происходит образование изомеров относительно положения альдегидного и кетонного атома углерода, что приводит к образованию смеси α – глюкопиранозы (36%) и β – глюкопиранозы (63%); оставшийся 1% представлен в основном α – и β – аномерами глюкофуранозы. Описанное выше установление равновесия сопровождается так называемой мутаротацией: полуацетальное кольцо раскрывается и вновь замыкается, при этом может изменяться положение групп – Н и – ОН при углероде 1. Предполагают, что в ходе этого процесса образуется промежуточная гидратированная линейная (ациклическая) молекула, хотя по данным полярографии на долю ациклической формы глюкозы приходится всего 0,0025%. В растворе глюкоза является правовращающей; этим объясняется еще одно ее название – декстроза (декстро – правый), часто употребляемое в клинической практике (Рисунок 4).
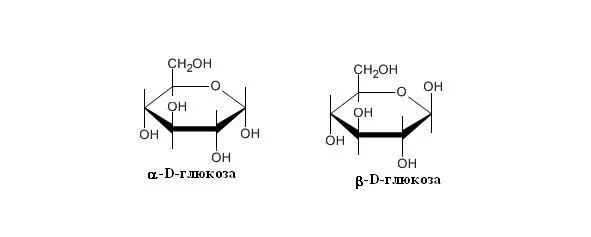
Рисунок 4. Структурные формулы аномеров глюкозы. α- и β-аномеры
4. Эпимеры.Изомеры, различающиеся по конфигурации положением групп – Н и – ОН при асимметричных атомах углерода, которые не связаны с принадлежностью к стереоизомерам, называются эпимерами. Биологически наиболее важными эпимерами глюкозы являются: манноза и галактоза, образующиеся путем эпимеризации при атомах углерода 2 и 4 соответственно (Рисунок 5).
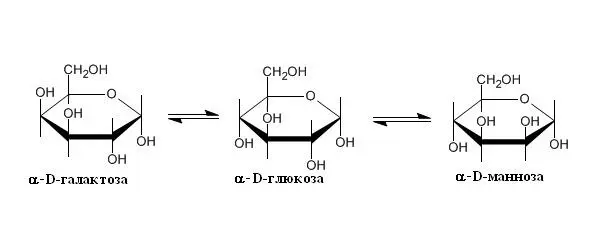
Рисунок 5. Эпимеризация глюкозы
5. Альдо-кето-изомеризация.Фруктоза имеет ту же химическую формулу, что и глюкоза, но отличается по структурной формуле, поскольку фруктоза содержит потенциальную кетонную группу в положении 2, а глюкоза – потенциальную альдегидную группу в положении 1.
Конформация моносахаридов
Шестичленные кольца из одинарных связей, в циклогексане и в сахарах, как правило, принимают конформацию «кресла», как это видно на примере глюкозы (Рисунок 6). Помимо этого, шестичленные кольца могут принимать менее устойчивую конформацию «лодки». Свободно переходят одна в другую через промежуточные скошенные конформации.
Пятичленные кольца образуют конформацию «конверта».
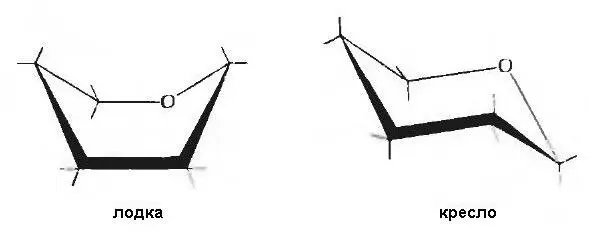
Рисунок 6. Конформация шестичленных колец
Физические свойства моносахаридов
Моносахариды гидрофильны, а, следовательно, легко растворимы в воде. Растворимость моносахаридов примерно одинакова, поэтому разделение моносахаридов достаточно сложно. Моносахариды не поглощают свет ни в видимой, ни в ультрафиолетовой части спектра. Из-за этого нельзя определять концентрацию моносахаридов спектрофотометрическими методами. Так как моносахариды находятся в природе либо в растворе, либо в кристаллах, в физиологических диапазонах температуры нет вопроса о температурах плавления и кипения.
Химические свойства моносахаридов
По своей структуре моносахариды содержат два типа функциональных групп: спиртовые и альдегидные (кетонные), соответственно моносахариды вступают в реакции по этим группам. Моносахариды вступают во многие химические реакции, весьма важные для практического использования и исследования углеводов. Реакции, обсуждаемые в данном разделе, демонстрируют либо наиболее важные свойства углеводов, либо типы реакций, часто встречающиеся в их метаболизме.
Образование эфиров. Это реакция спиртовых групп образуются либо эфиры неорганических кислот, либо органические эфиры (простые со спиртами или галогенидами или сложные с ангидридами кислот). Наиболее активной является полуацетальная спиртовая группа, соответственно она чаще вступает в реакции с образованием эфиров. Эфиры фосфорной и уксусной кислот занимают уникальное место в биохимии и встречаются во многих углеводах и их производных.
Читать дальше
















