Наряду с большими электромагнитными разделительными установками для промышленного производства изотопов широкое применение получили лабораторные сепараторы. Они используются для получения радиоактивных изотопов, необходимых для ядерной спектроскопии , для изучения взаимодействия ионов с твёрдым телом (при ионном внедрении и для других целей).
Другие методы разделения. Помимо перечисленных, существует ряд других методов, применение которых носит ограниченный характер или находится в стадии исследований или технических усовершенствований. К ним относятся: получение 3He, основанное на явлении сверхтекучести 4He; разделение посредством диффузии в сверхзвуковой струе газа, расширяющейся в пространстве с пониженным давлением; хроматографическое разделение, основанное на различии в скоростях адсорбции изотопов; биологические способы разделения.
Методы И. р. имеют особенности, определяющие области их наиболее эффективного применения. При И. р. лёгких элементов с массовыми числами около 40 экономически более выгодны и эффективны дистилляция, изотопный обмен и электролиз. Для разделения изотопов тяжёлых элементов применяются диффузионный метод, центрифугирование и электромагнитное разделение. Однако газовая диффузия и центрифугирование могут быть использованы, если имеются газообразные соединения элементов. Поскольку таких соединений мало, реальные возможности этих методов пока ограничены. Термодиффузия позволяет разделять изотопы как в газообразном, так и в жидком состоянии, но при разделении изотопов в жидкой фазе a мало. Электромагнитный метод обладает большим a, но имеет малую производительность и применяется главным образом при ограниченных масштабах производства изотопов.
Для обеспечения научно-исследовательских работ и практических применений изотопов в СССР создан Государственный фонд стабильных изотопов, обладающий запасом изотопов почти всех элементов. Регулярно производится разделение значительных количеств дейтерия 10B, 13C, 15N, 180, 22Ne и других изотопов. Организован также выпуск различных химических препаратов, меченых стабильными изотопами.
Лит.: Бродский А. И., Химия изотопов, М., 1952; Смит Г., Атомная энергия для военных целей, пер. с англ., М., 1946; Физический энциклопедический словарь, т. 4, М., 1965; Розен А. М., Теория разделения изотопов в колоннах, М., 1960; Джонс К., Ферри В., Разделение изотопов методом термодиффузии, пер. с англ., М., 1947; Koch J. [ed.], Electromagnetic isotope separators and applications of electromagnetically enriched isotopes, Amst., 1958.
В. С. Золотарев.

Рис. 7. Завод для электромагнитного разделения в Ок-Ридже (США).
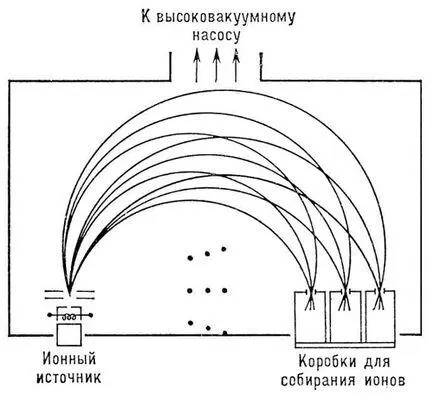
Рис. 6. Схематическое изображение электромагнитного разделительного устройства; точки показывают направление магнитного поля, перпендикулярное плоскости рисунка.
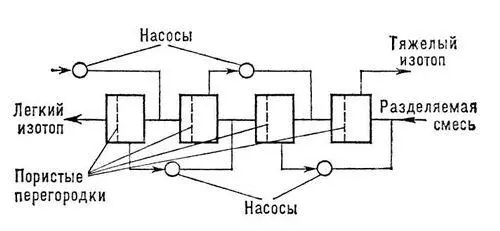
Рис. 1. Схема устройства для разделения изотопов методом газовой диффузии.
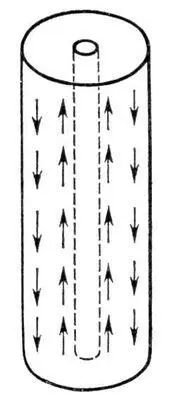
Рис. 5. Схема термодиффузионной разделительной колонки.

Рис. 2. Газодиффузионный завод для производства 235U в Ок-Ридже (США).
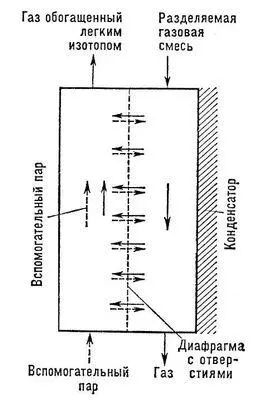
Рис. 3. Схема устройства для разделения изотопов методом противопоточной масс-диффузии.

Рис. 4. Разделительная установка, работающая на противопоточной масс-диффузии.
Изото'пы(от изо... и греч. tópos — место), разновидности одного химического элемента, занимающие одно место в периодической системе элементов Менделеева, но отличающиеся массами атомов. Химические свойства атомов, т. е. принадлежность атома к тому или иному химическому элементу, зависят от числа электронов и их расположения в электронной оболочке атома (см. Атом ). Место химического элемента в периодической системе элементов определяется его порядковым номером Z , равным числу электронов в оболочке атома или, что то же самое, числу протонов , содержащихся в атомном ядре. Кроме протонов, в ядро атома входят нейтроны , масса каждого из которых приблизительно равна массе протона. Количество нейтронов N в ядре атома с данным Z может быть различным, но в определённых пределах. Например, в ядре атома гелия ( Z = 2) может содержаться 1, 2, 4 или 6 нейтронов. Полное число протонов Z и нейтронов N в ядре (называется общим термином нуклоны) определяет массу ядра и по существу массу всего атома. Это число А = Z + N называется массовым числом атома. От соотношения чисел протонов и нейтронов в ядре зависят стабильность или нестабильность ядра, тип распада радиоактивного ядра, спин , магнитный дипольный момент, электрический квадрупольный момент ядра и некоторые другие его свойства (см. Ядро атомное ). Таким образом, атомы с одинаковым Z , но с различным числом нейтронов N обладают идентичными химическими свойствами, но имеют различные массы и различные ядерные свойства. Эти разновидности атомов также называются И. Для обозначения любых разновидностей атомов, независимо от их принадлежности к одному элементу, применяют термин нуклиды.
Читать дальше







