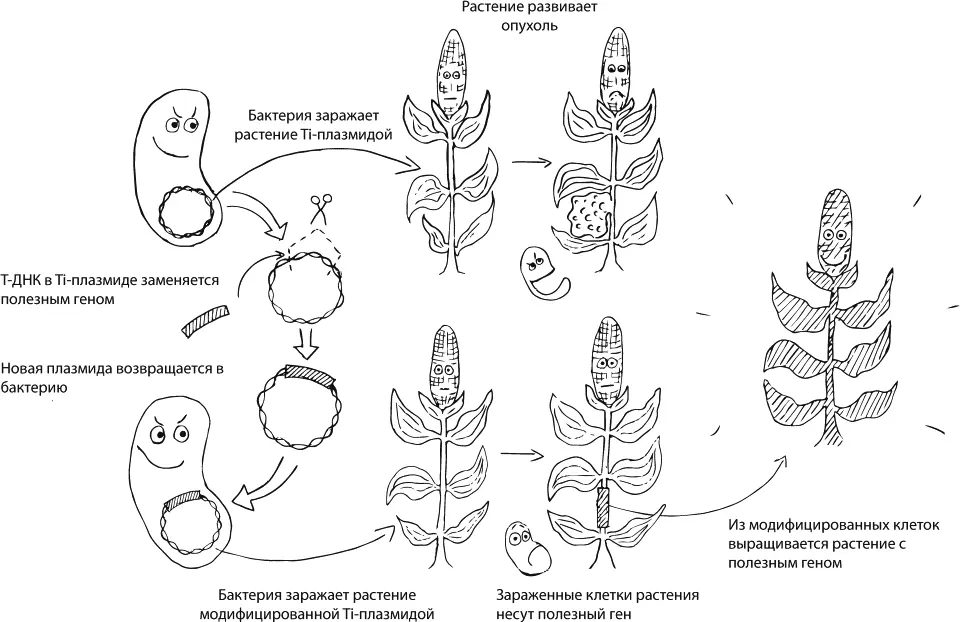
Генетики берут эту готовую конструкцию, выкидывают из нее все те гены, которые нужны бактерии, и вставляют те, которые нужны людям. Несчастная обманутая бактерия проделывает всю ту же самую работу, но модифицированная клетка растения уже не начинает бурно делиться и не производит опины – зато обладает теми свойствами, которые нужны нам. Потом из удачно модифицированной клетки, благодаря способности растений к вегетативному размножению, можно будет вырастить целый организм. Именно с помощью такого подхода получена, например, устойчивая к засухе кукуруза MON87460, которую интенсивно выращивают по обе стороны Атлантического океана. В нее был введен бактериальный ген cspB , отвечающий за производство РНК-шаперона – белка, предотвращающего неправильную укладку молекул РНК под действием стресса, в данном случае недостатка воды. Его присутствие помогает кукурузе выращивать нормальные семена, даже когда ее недостаточно поливают. По остальным экологическим и пищевым параметрам эта кукуруза не отличается от такой же, но немодифицированной [16], [17].
Главный недостаток агробактериальной трансформации (и других методик генной инженерии первого поколения) – это невозможность контролировать, в какое именно место в ДНК растения встроится новая конструкция. Вообще-то это не такая большая проблема: мы ведь получаем не единственное растение, а несколько. Если она где-то встроится так, чтобы это повлияло на остальные свойства растения, – исследователи это заметят. Если будут сомневаться – расшифруют ДНК, чтобы установить место локализации точно. Тем не менее, действительно, методы генной инженерии нового поколения направлены на то, чтобы встраивать новую ДНК не куда попало, а в заранее заданное место. Есть несколько способов делать это в пробирке, но главный писк моды сейчас – система CRISPR/Cas 9, позволяющая вставлять гены в заданное место прямо в живой клетке. Эта методика может не только упростить и удешевить получение новых генетически модифицированных животных и растений, но и привести к серьезным прорывам в медицине. Я уже упоминала ее в связи с вырезанием из человеческих клеток ДНК вируса иммунодефицита человека. Другая перспективная сфера применения – генная терапия, исправление ДНК человека для излечения наследственных заболеваний. Конечно, исследования и клинические испытания в этой области проводились и до появления CRISPR/Cas 9, в том числе вполне успешные, но она вполне может в обозримом будущем привести к переходу медицины на качественно новый уровень. И да, систему CRISPR/ Cas 9исследователи тоже позаимствовали у бактерий. Зачем она им? Не поверите, это их приобретенный иммунитет.
Мы все знаем со школьной скамьи, что приобретенные признаки не наследуются. Это, в общем, правильный принцип. Он остается верным и в том случае, если обретение нового признака привело к изменению генов – но не во всем организме, а в каких-то отдельных его клетках, не участвующих в размножении. Если вы переболели краснухой и у вас сформировался к ней иммунитет, то геном тех B-лимфоцитов, которые с ней боролись, изменился, пока они подстраивались под выработку оптимальных антител против данного вируса. Но у вашего ребенка все равно не будет иммунитета к краснухе, если только не пытаться клонировать его из соответствующей клетки иммунной памяти (честное слово, это плохая идея). Если почвенная агробактерия изменила клетки корня растения, чтобы они бурно размножались и вырабатывали опсины, потомки этого растения, выращенные из семян, все равно не будут этого делать: где корень, а где семена?
Но вот если генетически изменилась та самая клетка, из которой получится потомство, – это совсем другое дело. Приобретенные признаки наследуются, когда генные инженеры используют способность растений к вегетативному размножению и выращивают целый организм из модифицированной ими клетки корня. А в природе приобретенные признаки сплошь и рядом наследуются у одноклеточных существ. Все, что повлияло на геном бактерии, передается ее потомкам. Благодаря этому она может позволить себе завести самый настоящий приобретенный иммунитет, что едва ли имело бы смысл без его передачи по наследству (много ли вирусов успеет встретить бактерия за 20 минут своей жизни от деления до деления?).
Когда бактерия все-таки встречается с атакующим ее вирусом, она берет из его ДНК кусочек и встраивает в свой собственный геном – на память. Не куда попало, а между определенными генетическими последовательностями, которые называются CRISPR.
Читать дальше
Конец ознакомительного отрывка
Купить книгу













