А что означают цифирки после запятой?..
В обычном нормальном атоме золота, как мы уже выяснили, 117 нейтронов и 79 протонов. Но иногда встречаются атомы-уродцы. У них есть лишние нейтроны. Как иногда у людей бывает по шесть пальцев на руках. Нечастое явление.
Предположим, на тысячу нормальных атомов приходится один дефектный. И если в норме в атоме золота 117 нейтронов, то иногда встречаются «вспухшие» уродливые атомы, в которых 118 нейтронов. Атомы-уродцы называют изотопами. Именно из-за них средний вес всех атомов вещества отличается от целого числа. Что понятно: если у нас из десяти атомов все десять имеют атомный вес в 6 единиц, то и средний атомный вес будет равен ровно шести:
(6+6+6+6+6+6+6+6+6+6): 10 = 6
А вот если один из десяти атомов имеет вес в 7 единиц, средний вес изменится:
(6+6+6+6+6+7+6+6+6+6): 10 = 6,1
Видите, после запятой появилась цифирка, которая говорит о том, что не «все шестерки одинаковы».
Если вы внимательно посмотрите на атомные веса элементов в таблице Менделеева, то увидите, что все они не являются целыми числами. Значит, каждое элементарное вещество имеет уродливые атомы. Даже водород. Хотя, казалось бы, проще водорода ничего быть не может – один протон, вокруг которого крутится один электрон, вот и весь атом. Это не какой-нибудь свинец, у которого в ядре больше двух сотен нуклонов, а вокруг этого огромного ядра кружится более 80 электронов!.. Однако все же бывают атомы водорода, в ядре которых, кроме протона, есть еще и нейтрон. Один. А порой и два! Такой водород называют тяжелым. Потому что его атом тяжелее обычного.
На рисунке ниже нарисованы атомы нормального водорода и редкие уродики, а также написано, как эти уродики называются.
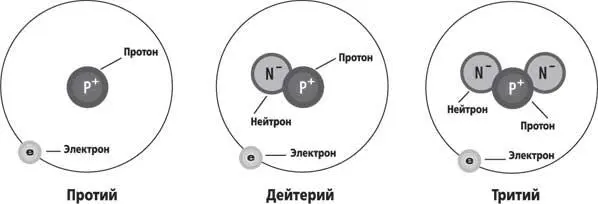
Обычный водород. Дейтерий. Тритий
Но так как атомы-уродцы встречаются редко, говорить мы о них пока прекращаем. А возьмем сейчас тот же хлор и натрий, из которого ранее соль поваренную делали, и посмотрим, что тут к чему.
Натрий. Легкий металл. Как он сделан? Его номер 11-й. Значит, 11 протонов и 11 электронов. Атомный вес натрия – 22. То есть в ядре 22 нуклона.
22 нуклона минус 11 протонов = 11 нейтронов.
Все. Атом натрия готов.
Теперь хлор надо собрать по инструкции дяденьки Менделеева.
У хлора номер 17. То есть 17 протонов и 17 электронов. Атомный вес (число нуклонов в ядре) – 35.
35 – 17 = 18 нейтронов.
Все, собрали хлор.
Теперь соединяем два этих атома – хлора и натрия, – зацепив один за другой колечками самых дальних электронных орбит, и получаем сложное вещество – молекулу поваренной соли.
Так строятся все вещества – сцепляясь дальними орбитами электронов. При этом дальние электрончики, которые крутились на этих орбитах, становятся как бы общими для обоих ядер.
Все, можно стереть пот со лба. Мы освоили химию и физику элементарных частиц. Слава Менделееву! Науке слава!
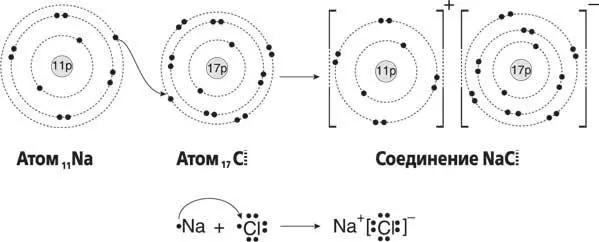
Молекула поваренной соли – хлорид натрия. Кушать подано!
Теперь осталась одна маленькая деталь, которую нужно знать каждому приличному гражданину. Один маленький штрих, который завершит картину мироздания, сделав ее в ваших блестящих глазах более полной и блестящей.
Итак, мы знаем, что практически все окружающее нас вещество электронейтрально. Если вы дотрагиваетесь до шкафа, он не бьет вас током. Потому что в веществе шкафа количество положительных зарядов равно количеству отрицательных. Его атомы электронейтральны.
Но что будет, если атом потеряет один или два электрона? Вот такой рассеянный атом. Может такое быть? Может! Какое-нибудь сильное воздействие может парочку электрончиков у атома оторвать.
Вы скажете (подсмотрев в таблицу Менделеева):
– Ха! Даже если такое случится, невелика потеря! Вокруг ядра атома могут крутиться под сотню электронов! Например, у радия их 88. Некисло так! Подумаешь, пару потеряет…
Однако потеря даже одного отрицательного заряда означает избыток заряда положительного. Если атом теряет электрон, значит, у него остается один «лишний», нескомпенсированный протон. И атом в целом, таким образом, приобретает положительный заряд +1.
А если атом теряет два электрона, то он приобретает заряд +2.
Бывает и наоборот – когда к атому присоседится какой-нибудь приблудный лишний электрон. В этом случае атом получает один отрицательный заряд –1.
Читать дальше












![Уильям Байнум - Краткая история науки [litres]](/books/412489/uilyam-bajnum-kratkaya-istoriya-nauki-litres-thumb.webp)

