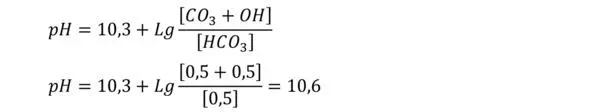1 ...6 7 8 10 11 12 ...23 2NaHCO 3 = Na 2CO 3+Н 2CO 3 свобод = Na 2CO 3+CO 2 газ+ Н 2О (6)
Полноту протекания данного процесса в деаэраторе можно оценить по значению рН воды после деаэратора. Значение рН воды после деаэратора будет определяться по отношению содержания карбонат-иона к гидрокарбонат-иону (уравнение Хендерсона-Хассельбальха для разложения бикарбоната HCO 3=H+CO 3)

К примеру, вода, содержащая 2 моля бикарбоната натрия (6), подвергается барботированию в деаэраторе. В результате отвода СО 2бикарбонат-ион переходит в карбонат-ион. В зависимости от интенсивности отвода СО 2на выходе из деаэратора в воде устанавливается равновесие между карбонатом и бикарбонатом, при этом происходит только разложение половины бикарбоната. Соответственно, в результате парового барботажа воды получаем содержание в ней 1 моля бикарбоната натрия, 0,5 моль карбоната натрия и 0,5 моль углекислого газа. Углекислый газ был отведен в атмосферу. Тогда в соответствии с (7) получаем:

Значение рН дегазированной воды после деаэратора получается 9,99. При этом в деаэраторе произведена отгонка только свободной углекислоты и разрушение и отгонка половины полусвязанной углекислоты (четвертая часть исходного бикарбоната).
Предположим, в деаэраторе разрушается не половина, а ¾ бикарбоната натрия. Тогда, получаем в результате отгонки углекислоты, остается одна четверть бикарботана, или 0,5 моля бикарбоната, и, соответственно, на 0,5 моля на карбонат, 0,5 моля на гидрат и 1 моль на углекислоту (которую отогнали в деаэраторе). В данном случае половину углекислоты удалили в деаэраторе от исходного количества бикарбоната. В данном примере в воде появляется гидрат в результате процесса гидролиза карбонатов. В данном случае уравнение (7) запишется следующим образом:
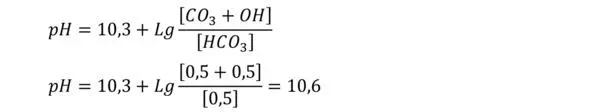
Процесс гидролиза бикарбонатов и карбонатов подробно рассмотрен в статье «Определение количества бикарбонатов, карбонатов и гидратов в воде в зависимости от значения рН воды».
Рассчитаем значение рН воды, которое необходимо получить на выходе из деаэратора, соответствующее равному (одинаковому) содержанию бикарбоната и карбоната, т.е. бикарбоната, карбоната и угольной кислоты будет равное количество – по 0,665 моля. 0,665*3= 2 моля исходного бикарбоната. Соответственно,

Значение рН=10,3 соответствует константе диссоциации бикарбоната по уравнению HCO 3<-> H+CO 3. Т.е. количество бикарбоната равно количеству карбоната. Можно сказать, что при данном рН воды половина бикарбоната подпиточной воды разложилась в деаэраторе, но при этом отогналась только третья часть общей суммы всех форм диоксида углерода (8).
0,665NaHCO 3= 0,665Na 2CO 3+0,665CO 2 газ+Н 2О ⠀⠀ (8)
– Третья стадия – продолжение отвода углекислоты из воды при интенсивном кипении, за счет чего карбонат гидролизируется с образованием углекислого газа и высвобождением гидроксил-иона из молекулы воды (9). Данный процесс не требует отвода углекислоты из воды. Это обычная реакция гидролиза технической соды в воде. Поэтому, вероятно, неправильно говорить о разрушении связанной углекислоты (карбоната) за счет отвода газообразной углекислоты. Скорее надо говорить о гидролизе технической соды в воде. Данные условия обеспечиваются как в деаэраторе, так и тем более в котле. Можно сказать, что скорость протекания реакции (9) лимитируется остаточным содержанием бикарбоната в воде, а не скоростью отвода углекислого газа в (9). А уже концентрация бикарбоната зависит от эффективности отвода растворенной углекислоты (6).
Na 2CO 3+ H 2O=2NaOH+ CO 2 газ ⠀⠀ (9)
Na 2CO 3+ H 2O=NaOH+ NaHCO 3 ⠀⠀ (10)
Считается, что чем выше температура и давление в котле, тем полнее происходит разложение карбонатов в котловой воде за счет условий, обеспечивающих чрезвычайно эффективный отвод углекислоты из воды. Полное разложение карбонатов получается в котлах при давлении 5 МПа [1]. Тем не менее автор считает, что разрушения карбонатов как такового нет. Происходит их гидролиз (9, 10). Соответственно, чем меньше бикарбоната в воде, тем полнее идет гидролиз карбонатов, и именно это определяет полноту разложения карбоната. Так, при работе парового котла на давлении 6 бар и подпитке котла обессоленной водой после обратного осмоса с щелочностью около 0,25 мг-экв/л в котловой воде фактически не обнаруживается бикарбонат и карбонат-ион. Только гидроксил (присутствует только фенолфталеиновая щелочность).
Читать дальше