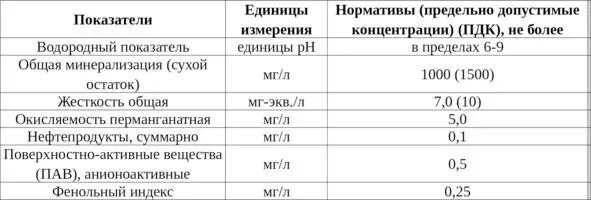
Таблица 4. Группа показателей – химические
рН – водородный показатель
Определение рН или водородного показателя воды – это вычисление значений показателя концентрации ионов гидроксония (водородных катионов), который математически равен отрицательному логарифму значения концентрации водородных ионов:
рН = -1g (Н +)
Молекулу воды относится к так называемым слабым электролитам. Степень ее собственной диссоциации на ионы (ион водорода Н + и гидроксильный ион ОН -) очень невелика. Произведение концентраций этих ионов называется ионным произведением воды Кw:
Kw = (H +) (OH -) = (10 —7) (10 —7) = 10 —14 (моль/л) 2
Так, оценивают, что из 10 млн. молекул воды только одна диссоциирует на ион водорода и гидроксильный ион:
Н 2О – ›Н + + ОН -
Деминерализованная чистая вода должна в идеале иметь значение рН ≈ 7.
Присутствие солей, содержащих катионы и анионы слабых кислот и оснований, оказывает сильное влияние на значение водородного показателя:
Mg 2+∙H 2O + H 2O ↔ MgOH + + H 3O +
CO 3 2- + H 2O ↔ HCO 3 - + OH - и т. д.
Таким образом, рН воды всегда определяется соотношением концентраций ионов, которые участвуют в кислотно-основном равновесии для данной пробы воды. Если концентрация образующихся гидроксильных ионов выше, чем концентрация ионов водорода, то показатель рН имеет значение больше 7 и среда характеризуется, как щелочная. Если выше концентрация ионов водорода (ионов гидроксония), то pH меньше 7 и среда характеризуется, как кислая. Общие требования к качеству воды приведены в гигиенических нормативах [37,38].
Соответственно, активная реакция воды в зависимости от концентрации водородных ионов может быть нейтральной, кислой или щелочной (табл. 5).
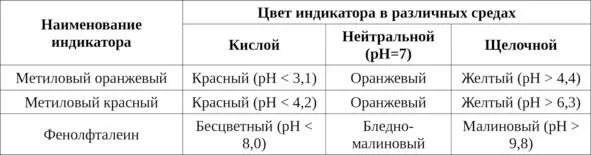
Таблица 5. Определение рН индикаторным способом
Показатель – общая минерализация
Показатель общей минерализации характеризует суммарную концентрация всех ионов (анионов, катионов) и недиссоциированных соединений, а также растворенных в воде органических веществ, которая имеет единицы измерения грамм на литр (г/л) или на кубический дециметр (г/дм 3).
Фактически, общая минерализация при определении в воде может быть по значению близка с показателем «сухой остаток», который анализируют посредством выпаривания пробы воды определенного объема, которую предварительно профильтровывают через бумажный фильтр, а далее высушивают при температуре 105—120 °С до постоянного веса. Следует учесть, что сухой осадок не учитывает фракцию отогнанных при выпаривании органических соединений. Сухой остаток можно рассчитать также путем суммирования приведенных значений концентраций анионов и катионов, определенных различными методами химического анализа. По действующим нормативам общая минерализация питьевой воды не должна превышать 1 г/л. [37,38,43, 44—46]
Показатель – жесткость воды
Наличие жесткости воды обусловлено присутствием в любой воде катионов некоторых металлов, в том числе: кальция (Са 2+), магния (Mg 2+), стронция (Sr 2+), бария (Ва 2+), железа (Fe 2+, Fe 3+), марганца (Mn 2+) и некоторых других.
Вследствие того факта, что показатели значения концентрации ионов кальция и магния для воды естественного происхождения практически во всех случаях выше, чем для ионов других металлов, общее значение показателя жесткости определяют, основываясь на анализе концентраций именно катионов кальция и магния. В целом, значение общей жесткости определяется приведенным сложением значений карбонатной (временной, устраняемой кипячением) и некарбонатной (постоянной) жесткости. В свою очередь, постоянная жесткость вызывается присутствием в воде кальция и магния в виде сульфатов, хлоридов, силикатов, фосфатов.
Жесткость воды, вызванная наличием катионов кальция и магния, связана с процессами образования с присутствующими в воде карбонатными и гидроксильными ионами малорастворимых соединений кальция и магния. Имеющиеся в природных водах гидрокарбонатные анионы при повышении температуры разлагаются на углекислый газ и ион угольной кислоты:
2Н 2СО 3—›СО 2+СО 3 2-+Н 2О
В том случае, если в воде присутствуют катионы жесткости, при взаимодействии с карбонатными анионами при высоких температурах происходит образование солей с очень низкой растворимостью. Таким образом воды с высокой жесткостью могут образовывать накипь и отложения на разного рода бытовой технике, котлах при нагревании и в трубопроводах горячей воды. Точно также катионы жесткости образуют труднорастворимые соли с жирными кислотами, которые входят в состав различных моющих средств, что зачастую является существенной помехой при использовании жесткой воды для разных видов стирки.
Читать дальше
Конец ознакомительного отрывка
Купить книгу














