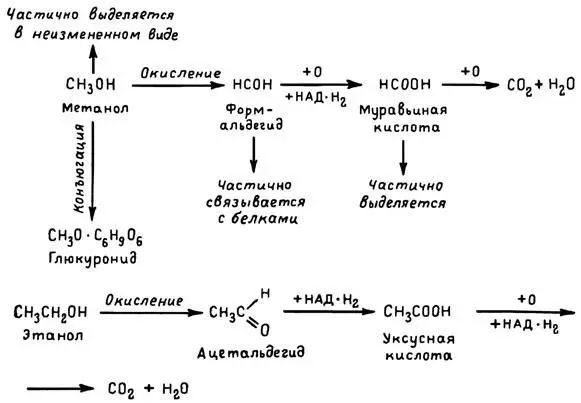
Рис. 19. Биотрансформация метилового и этилового спиртов. НАД — никотинамидадениндинуклеотид, кофермент дегидрогеназы, обеспечивающий перенос водорода при окислительно-восстановительных реакциях
Вмешательство в биохимические процессы обмена ядовитых веществ возможно и с помощью ферментных препаратов заместительного действия. Здесь в первую очередь надо вспомнить те ферменты, ингибирование которых при отравлениях определяет существо механизма действия ядов. Мы уже имели возможность убедиться, что введение в организм отравленного препаратов, включающих каталитически активные компоненты ферментов (моноаминоксидазы, пируватоксидазы), является весьма действенным лечебным приемом. В связи с этим несомненный антидотный интерес представляют препараты, включающие целые молекулы ингибируемых ферментов. Одна из первых попыток в данном направлении связана с холинэстеразой, очищенный препарат которой был предложен еще в 1952 г. шведским ученым Аугустинссоном для борьбы с отравлением ФОС. В 1961 г. в США специалисты одной исследовательской лаборатории пришли к выводу о возможности использования электрических угрей как источника холинэстеразы. Оказалось, что в организме этих рыб содержится весьма большое количество фермента. В 1970 г. сотрудниками Института эволюционной физиологии и биохимии им. И. М. Сеченова (г. Ленинград) был разработан метод получения холинэстеразы из эритроцитов крови быка. Тогда же была налажена технология ее промышленного получения с учетом возможного использования в клинике. Надо, однако, иметь в виду, что, кок и любой другой ферментный белок, холинэстераза слабо проникает в ткани нервной системы, с это, естественно, снижает ее лечебное действие.
Если фермент ускоряет обезвреживание яде, то дополнительное его впадение в организм должно затормозить течение интоксикации. Таким действием, к примеру, обладает роданаза. Было доказано, [205] Sorbо В. Treatment of chemical warfare casualties. — Rev. lnternationale des services de Sante des Armeesde Terre, de Мer. et de Y'Air, 1963, № 2, p. 82–89.
что на фоне цианидного отравления этот фермент значительно усиливает дезинтоксикационное роданообразование тиосульфатом натрия и другими донаторами серы.
Иное использование ферментов при интоксикациях связано с их способностью вступать в конкурентные отношения с той или иной биоструктурой за связь с ядом или же непосредственно взаимодействовать с его молекулами. Тем самым ферментный препарат как бы принимает удар на себя. Данный механизм защитного действия можно видеть на примере использования протеолитических, т. е. расщепляющих белки, ферментов — химотрипсина и трипсина — при отравлениях ФОС. Установлено, что эти ферменты очень чувствительны к фосфорорганическим ингибиторам и вступают с ними, подобно холинэстеразе, в реакцию фосфорилирования. [206] Бернхард С. Структура и функция ферментов / Пер. о англ. под ред. акад. А. Е. Браунштейна. М.; Мир, 1971.
Несомненный интерес в связи с этим представляют результаты экспериментального исследования, показавшего, что панкреатин (препарат, содержащий трипсин и амилазу, — пищеварительные ферменты поджелудочной железы) обладает выраженными антидотными свойствами по отношению к ряду высокотоксичных ФОС (октаметилу, хлорофосу и др.). [207] Абрамова Ж. И., Болтушкина Л. А. Защитный эффект панкреатива при экспериментальном отравлении фосфорганическими инсектицидами. — В кн.: Вопросы лечения профессиональных заболеваний и интоксикации. Л., 1937, с. 107–111.
На основании этих данных таблетки панкреатина по 0,2–0,5 г и аэрозоли трипсина предлагается использовать в качестве специфического средства профилактики профессиональных отравлений ФОС. Наряду с другими антидотами некоторые авторы рекомендуют применять их также и при появлении признаков интоксикации.
Как уже указывалось, окись углерода имеет особое сродство к ферропротеидам, содержащим двухвалентное железо, в тем числе и к дыхательным ферментам — цитохромам. Отсюда практическая ценность полученного в лаборатории профессора Л. А. Тиунова доказательства антидотных свойств цитохрома С при отравлении окисью углерода. [208] Тиунов Л. А., Васильев Г. А. К вопросу о применении цитохрома С для лечения острого отравления окисью углерода, — Фармакол, и токсикол., 1962, № 4, с. 483–484.
В чистом виде цитохром С впервые был выделен в 1935 г. из сердечной мышцы быка. Из 100 кг сердечной мышцы удалось получить 1 г цитохрома. Интересно отметить, что содержание железа в этом препарате (0,34%) было таким же, как и в гемоглобине. [209] Teorell А. Н. Kristallinisches Myoglobin. I. Kristallisiren und Reinigung des Myoglobins, sowie vorläufige Mitteilung über sein Molekulargewicht. — Bioch. Z., 1935, Bd 252, S. 1–7.
Предполагалось, что антидотное действие цитохрома С является следствием насыщения организма железом, содержащимся в этом препарате. Однако исследования итальянских ученых, проведенные в 1957–1959 гг., показали, что железо выполняет защитную роль при отравлении СО в дозировках, превышающих в пересчете на содержание Fe 2+в 30 раз лечебные дозы цитохрома С. К тому же было установлено, что поступающий извне цитохром выводится из организма в неизмененном виде. Тем самым, по-видимому, подтверждается мысль о заместительном лечебном действии этого фермента тканевого дыхания. [210] Клинические наблюдения показали, что в дозе 15–60 мг цитохром С достаточно эффективен при лечении отравленных СО (Рашевская А. М., Зорина Л. А. Профессиональные заболевания системы крови химической этиологии. М.: Медицина, 1968). Недавно на заводе медицинских препаратов (г. Ленинград) было налажено производство препарата цитохрома С как лекарственного средства широкого спектра действия. Получены убедительные данные о благотворном его влиянии на течение ряда заболеваний: инфаркта миокарда, печеночной комы, атрофии сетчатки глаза, расстройств кислотно-щелочного равновесия и др. (Правда, 1979, 26 сентября).
Читать дальше