Наша жизнь протекает в относительно мало меняющихся условиях. Давление воздуха колеблется в пределах нескольких процентов около одной атмосферы; температура воздуха, скажем, в районе Москвы лежит в интервале от -30 до +30°С; в абсолютной шкале температур, в которой за нуль принята самая низкая возможная температура (-273°С); этот интервал будет выглядеть менее внушительно: 240-300 К, что также составляет всего ±10% от средней величины.
Вполне естественно, что мы привыкли к этим обычным условиям и поэтому, говоря простые истины вроде: "железо - твердое тело, воздух - газ" и т. д., мы забываем добавить: "при нормальных условиях".
Если нагревать железо, оно сначала расплавится, а потом испарится. Если воздух охлаждать, то он сначала превратится в жидкость, а затем затвердеет.
Даже если читатель и не встречался никогда с железным паром и твердым воздухом, он, вероятно, без труда поверит, что любое вещество, изменением температуры можно получать и в твердом, и в жидком, и в газообразном состояниях, или, как еще говорят в твердой, жидкой или газообразной фазах.
Поверить в это легко потому, что одно вещество, без которого жизнь на Земле была бы невозможной каждый наблюдал и в виде газа, и как жидкость, и в виде твердого тела. Речь идет, конечно, о воде.
При каких же условиях происходят превращения вещества из одного состояния в другое?
Если опустить термометр в воду, которая налита в чайник, включить электроплитку и следить за ртутью термометра, то мы увидим следующее: почти сразу же уровень ртути доползет кверху. Вот уже 90, 95, наконец 100°С. Вода закипает, и одновременно прекращается подъем ртути. Вода кипит уже много минут, но уровень ртути не изменяется. Пока вся вода не выкипит, температура не изменится (рис. 4.1).
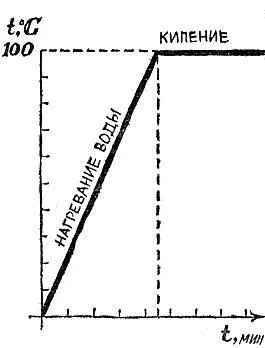
Рис. 4.1
На что же идет тепло, если температура воды не меняется? Ответ очевиден. Процесс превращения воды в пар требует энергии.
Сравним энергию грамма воды и грамма образовавшегося из нее пара. Молекулы пара расположены дальше одна от другой, чем молекулы воды. Понятно, что из-за этого потенциальная энергия воды будет отличаться от потенциальной энергии пара.
Потенциальная энергия притягивающихся частиц уменьшается с их сближением. Поэтому энергия пара больше энергии воды, и превращение воды в пар требует энергии. Этот избыток энергии и сообщается электроплиткой воде кипящей, в чайнике.
Энергия,- нужная для превращения воды в пар,; называется теплотой испарения. Для превращения 1 г воды в пар требуется 539 кал (это цифра для температуры 100°С).
Если 539 кал идет на 1 г, то на 1 моль воды будет затрачено 18*539 = 9700 кал. Такое количество тепла надо затратить на разрыв межмолекулярных связей.
Можно сравнить эту цифру с величиной работы необходимой для разрыва внутримолекулярных связей. Для того, чтобы 1 моль водяного пара расщепить на атомы, требуется около 220 000 кал, т. е. в 25 раз больше энергии. Это непосредственно доказывает слабость сил, связывающих молекулы друг с другом, по сравнению с силами, стягивающими атомы в молекулу.
Зависимость температуры кипения от давления
Температура кипения воды равна 100°С; можно подумать, что это неотъемлемое свойство воды, что вода,где бы и в каких условиях она ни находилась, всегда будет кипеть при 100°С.
Но это не так, и об этом прекрасно осведомлены жители высокогорных селений.
Вблизи вершины Эльбруса имеется домик для туристов и научная станция. Новички иногда удивляются, "как трудно сварить яйцо в кипятке" или "почему кипяток не обжигает". В этих условиях им указывают, что вода кипит на вершине Эльбруса уже при 82°С.
В чем же тут дело? Какой физический фактор вмешивается в явление кипения? Какое значение имеет высота над уровнем моря?
Этим физическим фактором является давление, действующее на поверхность жидкости. Не нужно забираться на вершину горы, чтобы проверить справедливость сказанного.
Помещая подогреваемую воду под колокол и накачивая или выкачивая оттуда воздух, можно убедиться, что температура кипения растет при возрастании давления и падает при его уменьшении.
Вода кипит при 100°С только при определенном давлении - 760 мм рт. ст. (или 1 атм).
Кривая температуры кипения в зависимости от давления показана на рис. 4.2. На вершине Эльбруса давление равно 0,5 атм, этому давлению и соответствует температура кипения 82°С.
Читать дальше