Самый важный для нас способ взаимодействия атомов называется ковалентной связью (см. рис. 1.1Б). Это связь, образуемая общей парой электронов — по одному от каждого из двух атомов. Можно считать, что электроны этой пары принадлежат обоим атомам сразу. На графических формулах, отображающих строение молекул наглядно, ковалентную связь обозначают простой чертой между символами химических элементов. Именно такими связями и соединены атомы в большинстве обычных молекул. Пример — молекула водорода. Она состоит из двух атомов водорода (H), образующих единственную ковалентную связь между собой: H−H, или сокращенно H 2.
Иногда ковалентные связи бывают двойными — образованными сразу двумя парами электронов — или даже тройными — образованными сразу тремя парами. Чем выше кратность связи, тем эта связь при прочих равных условиях прочнее. Двойные ковалентные связи встречаются в биологии очень часто. Тройные — намного реже, но знать об их существовании все-таки не помешает. На графических формулах двойные и тройные связи обозначают, соответственно, двойными или тройными черточками между символами атомов. Например, между атомами кислорода (O) вполне может образоваться двойная связь. В результате получится молекула O=O, или сокращенно O 2. Кстати, это и есть тот самый атмосферный кислород, которым мы дышим.
Гораздо реже ковалентной (по крайней мере, в живой материи) встречается ионная связь , представляющая собой электростатическое притяжение заряженных частиц. Мы уже знаем, что по закону Кулона одноименные электрические заряды отталкиваются, а разноименные — притягиваются. Поэтому положительно заряженная частица (катион) и отрицательно заряженная (анион) обязательно притянутся друг к другу. Уже упоминалось, что ионом называется любая самостоятельно существующая частица, в которой число электронов отличается от числа протонов. Сам этот термин, предложенный Майклом Фарадеем, происходит от греческого слова, означающего «идущий»: в растворе, через который пропущен электрический ток, положительно заряженные ионы движутся к отрицательному полюсу, а отрицательные — к положительному Атом становится ионом, если он приобрел лишний электрон или, наоборот, часть своих электронов где-то потерял.
Отличный пример ионной связи демонстрирует всем известная поваренная соль NaCl (натрий хлор), формулу которой можно переписать как [Na +][Cl −]. Это означает, что кристалл соли состоит из положительно заряженных ионов натрия и отрицательно заряженных ионов хлора в соотношении один к одному. В данном случае каждый атом хлора как бы отбирает один электрон у соседнего атома натрия.
Химический состав живой материи довольно однообразен. Для того чтобы в первом приближении разобраться в устройстве живой клетки, достаточно знать всего-навсего пять химических элементов. Это водород (H), кислород (O), азот (N), углерод (C) и фосфор (P). На атомные номера этих элементов мы пока не будем обращать внимания: во-первых, нет ничего легче, чем найти их в таблице Менделеева, а во-вторых, для нас сейчас гораздо важнее другой показатель. Самое главное, что нам нужно знать о любом химическом элементе, — это его валентность , то есть число ковалентных связей, которые может образовать его атом.
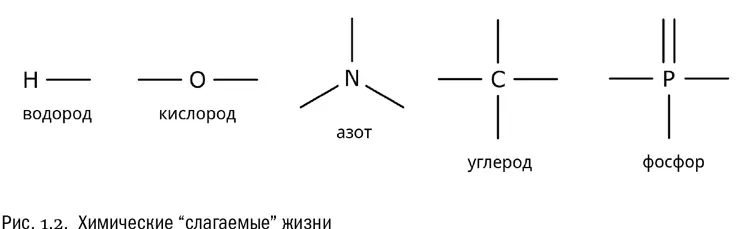
Итак, валентность водорода равна 1, кислорода — 2, азота — 3, углерода — 4 и фосфора — 5. Эти числа надо просто запомнить. Иногда у некоторых из перечисленных элементов бывают и другие валентности, но, занимаясь биологией, это можно игнорировать во всех случаях, кроме немногих особо оговоренных. Одновалентный водород, двухвалентный кислород, трехвалентный азот, четырехвалентный углерод и пятивалентный фосфор — главные химические слагаемые жизни (см. рис. 1.2).
Иногда по ходу разговора нам будут встречаться и другие атомы, например сера (S), натрий (Na), хлор (Cl), калий (K) или железо (Fe). Но постоянно помнить о них не надо. Пяти главных биогенных (то есть образующих жизнь) химических элементов для начала вполне достаточно.
Не подлежит сомнению, что большинство атомов в нашей Вселенной — это атомы водорода и гелия. Астрофизики утверждают, что 13 миллиардов лет назад, то есть «всего лишь» через несколько сот миллионов лет после Большого взрыва, соотношения были следующими: примерно 75 % всех атомов во Вселенной составляли атомы водорода, примерно 25 % — атомы гелия, а на атомы всех более тяжелых элементов, вместе взятых, приходилось 0,00007 % [7] Caffau E. et al. An extremely primitive halo star // arXiv preprint arXiv: 1203.2612 (2012).
. Конечно, с тех пор Вселенная изменилась. Но и сейчас все элементы, кроме водорода и гелия, составляют в сумме не больше 2 % существующих атомов. Между тем очевидно, что из водорода, валентность которого равна единице, и гелия, который вообще неохотно образует химические связи, никаких сложных молекул не построишь.
Читать дальше
Конец ознакомительного отрывка
Купить книгу











