1) содержание СО 2избыточное против равновесного, т.н. агрессивный оксид углерода ( IV);
2) степень насыщенности воды карбонатом кальция, т.е. величина
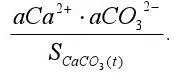
В основе расчета карбонатной системы различных природных вод лежат одни и те же уравнения (таблица 1).
Таблица 1.
Уравнения для расчета карбонатно-кальциевого равновесия [2]
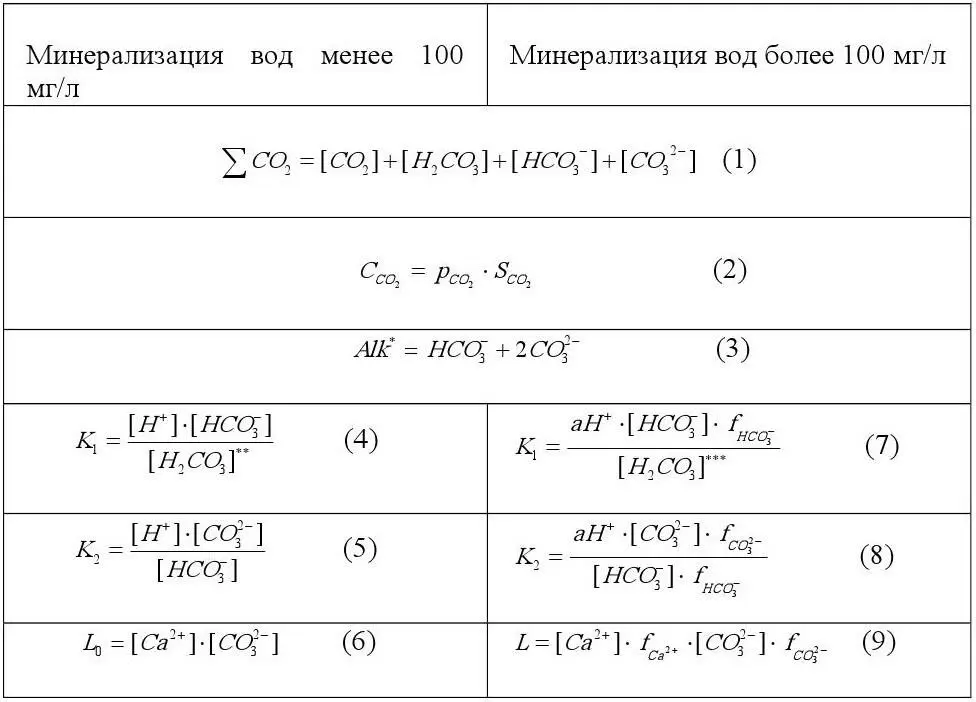
Примечание.
ΣCO 2– общее содержание компонентов карбонатной системы;
C CO2– концентрация свободного диоксида углерода;
P CO2 –парциальное давление СО 2;
S CO2– растворимость СО 2при данной температуре и давлении 10 5Па;
Alk – карбонатная щелочность;
[C i] – концентрация ионов;
[C i]f i– активность ионов;
aH +– активность ионов водорода;
f i– коэффициенты активности ионов;
к 1и к 2– термодинамические константы, соответственно, первой и второй ступени диссоциации угольной кислоты;
L 0– термодинамическое произведение растворимости СаСО 3;
L – произведение активноcти СаСО 3.
* При анализе получают общую щелочность
Alk общ= НСО 3 -+ 2СО 3 2-+ НSiO 3 -+ H 2BO 3 -+ HS -+ HPO 4 2-+ OH –+ H +
Однако карбонатная щелочность настолько близка к общей, что в большинстве случаев их не разделяют из-за малой концентрации других составляющих.
** Под концентрацией Н 2СО 3подразумевается общая концентрация растворенного СО 2(СО 2+ Н 2СО 3); тем самым допускается, что растворенный СО 2находится в виде Н 2СО 3.
*** Для недиссоциированной Н 2СО 3коэффициент активности равен единице.
Определение концентрации ионов водорода ( рН )
Величина рН природных вод определяется непосредственно у объекта. В последнее время для определения концентраций водородных ионов на сети станций Госкомгидромета стали применяться электрометрические портативные установки с использованием стеклянного электрода. Однако для работы в полевых условиях все еще основным методом определения рН является колориметрический метод. Из колориметрических методов наиболее надежным является метод с буферными растворами [3]. В значения рН необходимо вносить соответствующие значения солевых и температурных поправок. Наиболее удобной формой выражения величины рН можно считать формулу, предложенную К.Бухом [4]:
РН b= рН полев.+ ΔрН s+ ΔрН t+ α(t b– t' w) – γ(t’ w– t w), (10)
где: рН b– величина, определенная колометрическим методом с внесенными солевой и температурными поправками;
рН полев.– величина, определенная колометрическим методом;
ΔрН s– солевая поправка, зависящая от минерализации воды;
ΔрН s– поправка для приведения значений шкалы рН к температуре 18 оС (табл.2,3).
α(t b– t' w) – поправка на разность температур буферных растворов и пробы в момент определения рН;
t b– температура буферного раствора шкалы рН;
t' w– температура пробы в момент определения рН;
t w– температура воды в момент ее взятия;
γ(t’ w– t w) – поправка на разность температур в момент определения рН и в момент взятия пробы;
α – температурный коэффициент видимого изменения рН, отвечающий изменению константы диссоциации индикатора.
Конец ознакомительного фрагмента.
Текст предоставлен ООО «ЛитРес».
Прочитайте эту книгу целиком, на ЛитРес.
Безопасно оплатить книгу можно банковской картой Visa, MasterCard, Maestro, со счета мобильного телефона, с платежного терминала, в салоне МТС или Связной, через PayPal, WebMoney, Яндекс.Деньги, QIWI Кошелек, бонусными картами или другим удобным Вам способом.











![Николай Торицын - Краткое руководство по добыче и очистке воды в природных условиях [Учебное пособие]](/books/437851/nikolaj-toricyn-kratkoe-rukovodstvo-po-dobyche-i-och-thumb.webp)

