Возможно применение смешанных ангидридов. Так, для формилирования иногда используют смешанный ангидрид муравьиной и уксусной кислот, поскольку галогенангидриды и ангидрид муравьиной кислоты неустойчивы. В качестве ацилирующих агентов используются и сами карбоновые кислоты, а также их эфиры и амиды. В целом, по ацилирующей способности указанные агенты можно расположить в ряд:
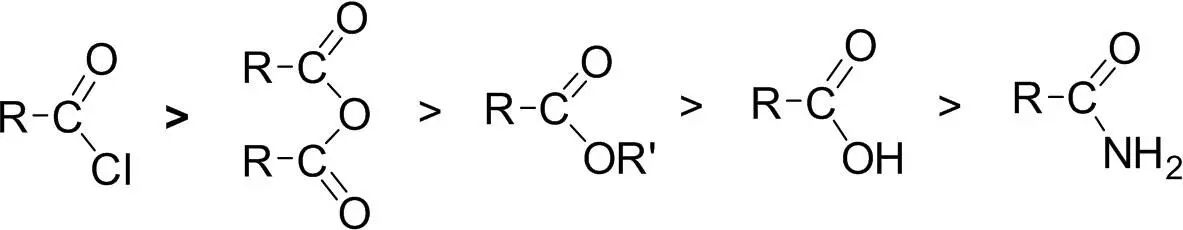
Чаще всего ацилированию подвергают соединения с подвижным водородом – амины, спирты, фенолы, тиоспирты и тиофенолы, например:
н-C 3H 7NH 2+ (CH 3CO) 2O н-C 3H 7NHCOCH 3+ CH 3COOH
н-C 3H 7OH + CH 3COCl → н-C 3H 7OCOCH 3+ HCl
C 6H 5SH + CH 3COCl → C 6H 5SCOCH 3+ HCl
Если в реакции ацилирования выделяется сильная кислота (например, НСl), то ее целесообразно связать, прибавляя в реакционную смесь такие основания, как сода, поташ, триэтиламин или пиридин.
Механизм реакции представляет собой присоединение нуклеофила (амин, спирт, тиол и т. п.) к карбонильной группе ацилирующего агента с последующим элиминированием из продукта присоединения протона и так называемой уходящей группы, находящейся в исходном ацилирующем средстве:
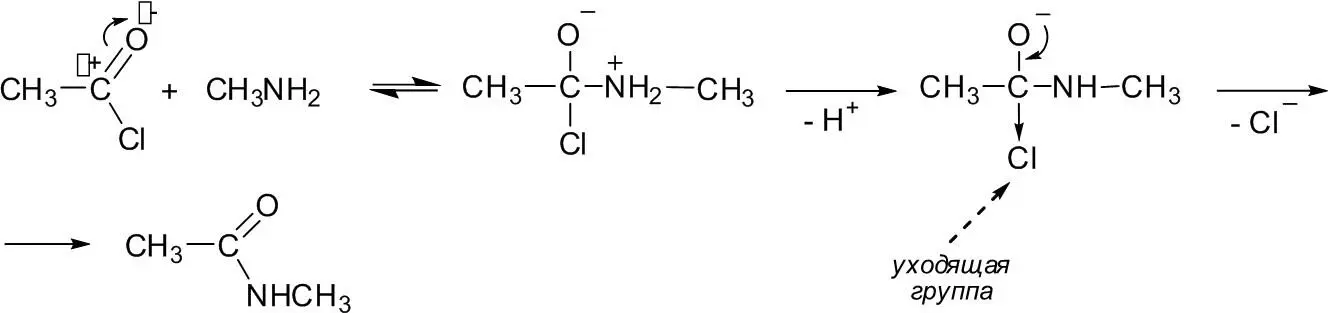
При одинаковых внешних условиях легкость ацилирования определяется, главным образом, тремя факторами: величиной положительного заряда на карбонильном атоме углерода, легкостью отщепления уходящей группы и нуклеофильностью соединения, которое ацилируют. Сочетание двух первых факторов дает тот ряд активности ацилирующих средств, который приведен выше. Так, аминогруппа менее электроотрицательна, чем хлор или оксигруппа, поэтому она не создает на карбонильном атоме углерода в амидах кислот достаточно большого положительного заряда; напротив, она этот заряд даже уменьшает за счет более сильного по сравнению с хлором и гидроксигруппой смещения неподеленной пары электронов азота к карбонильному углероду (+М-эффекта):
С другой стороны, в промежуточном продукте присоединения типа 1отщепление аминогруппы протекает значительно труднее, чем аниона Сl –или OH -, так как анион NH 2 –более нуклеофилен. Таким образом, эти обстоятельства не способствуют проявлению амидами кислот высокой ацилирующей способности, но благоприятствуют ей в случае хлорангидридов и ангидридов кислот.
В качестве ацилирующих средств нередко используют внутренние ангидриды таких дикарбоновых кислот, как янтарная или фталевая:
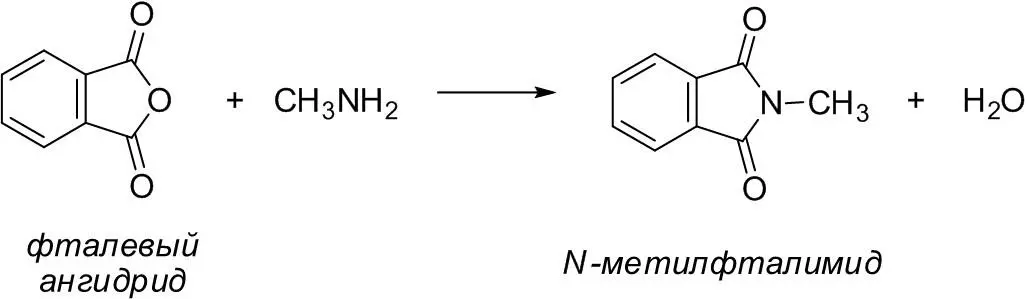
Ацилирование широко применяется в органической химии для защиты легко окисляющихся или просто активных функциональных групп. Так, анилин удобно нитровать в виде ацетанилида, поскольку сам анилин при действии азотной кислоты легко окисляется; кроме того, протонирование анилина увеличивает процент мета-замещения.
Для удаления ацильной защиты обычно используют кислотный или щелочной гидролиз или действие гидразина. Эти превращения, как и ацилирование, представляют собой нуклеофильное присоединение – элиминирование у карбонильного кислорода и с точки зрения механизма имеют много общего:
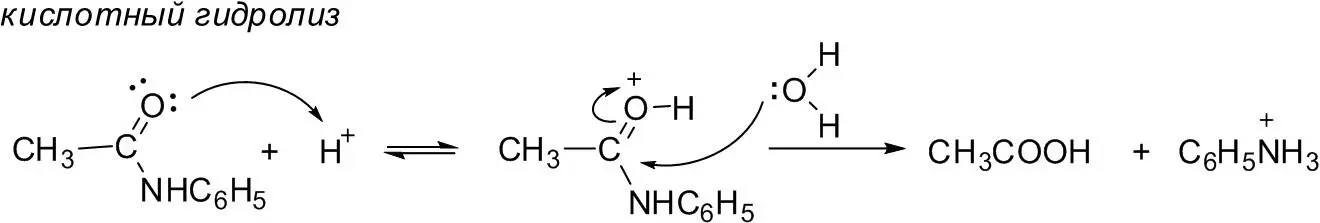
Фактически к реакциям ацилирования относится и этерификация карбоновых кислот спиртами, приводящая к образованию сложных эфиров:
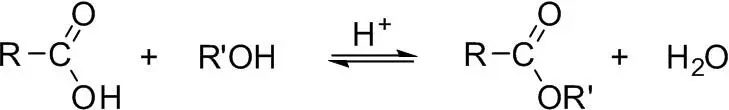
Эксперименты с исходными соединениями, меченными изотопом О 18, показали, что гидроксил в этой реакции отщепляется от кислоты, а не от спирта. Важную роль при этерификации играет кислотный катализ, поэтому в реакционную смесь обычно добавляют некоторое количество серной кислоты. Механизм кислотного катализа подробно рассмотрен в учебниках. Следует заметить, что реакция этерификации обратима: для ее смещения вправо требуется большой избыток спирта, тогда как гидролизу эфира способствует прибавление в смесь воды. Другие методы получения сложных эфиров – действие алкилгалогенидов на металлические соли карбоновых кислот, а также ацилирование спиртов хлорангидридами или ангидридами кислот.
Читать дальше










![Бекки Рапинчук - Органическая уборка для безопасности всей семьи. Дом без химии [litres]](/books/396861/bekki-rapinchuk-organicheskaya-uborka-dlya-bezopasnost-thumb.webp)





